Этилбензол
| Этилбензол | |
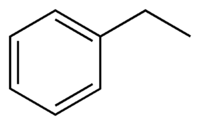 | |
 | |
| Общие | |
|---|---|
| Химическая формула | C8H10 |
| Физические свойства | |
| Молярная масса | 106.167 г/моль |
| Плотность | 0.8665 г/см³ |
| Термические свойства | |
| Температура плавления | -95 °C |
| Температура кипения | 136 °C |
| Химические свойства | |
| Растворимость в воде | 0.15 г/100 мл |
| Классификация | |
| Рег. номер CAS | 100-41-4 |
| SMILES | c1ccccc1CC |
Этилбензо́л — органическое вещество класса углеводородов.
Содержание
Свойства
Бесцветная жидкость; почти нерастворим в воде, растворяется в спирте, бензоле, эфире, четыреххлористом углероде.
Получение
Этилбензол содержится в нефти и каменноугольной смоле. В промышленности получают главным образом из бензола и этилена (по реакции Фриделя — Крафтса). Второй по значимости метод — выделение из С8-фракции продуктов риформинга.
Применение
При пропускании паров этилбензола над катализаторами образуется стирол, являющийся сырьём при производстве важных промышленных продуктов — некоторых видов пластмасс (см. Полистирол) и синтетических каучуков. Этилбензол используют также в органическом синтезе, например для получения ацетофенона жидкофазным каталитическим окислением, как растворитель и компонент высокооктановых бензинов.
Токсичность
Предельно допустимая концентрация паров этилбензола в воздухе 0,02 мг/м³
Полезное
Смотреть что такое «Этилбензол» в других словарях:
этилбензол — этилбензол … Орфографический словарь-справочник
этилбензол — сущ., кол во синонимов: 3 • растворитель (67) • углеводород (77) • фенилэтан (1) … Словарь синонимов
ЭТИЛБЕНЗОЛ — (C6H5C2H5) бесцветная жидкость. Содержится в нефти и продуктах коксования углей. Является сырьем для получения стирола, компонентом моторных топлив. Используют как растворитель … Российская энциклопедия по охране труда
этилбензол — бесцветная жидкость, tкип 136,2°C. Содержится в нефти и продуктах коксования углей. Сырьё для получения стирола; компонент моторных топлив, растворитель. * * * ЭТИЛБЕНЗОЛ ЭТИЛБЕНЗОЛ, С6Н5С2Н5, бесцветная жидкость, tкип 136,2 °С. Содержится в… … Энциклопедический словарь
ЭТИЛБЕНЗОЛ — ароматич. углеводород; бесцв. жидкость, tкип 136,2 °С. Содержится в нефти и продуктах коксования углей. Сырьё для получения стирола; компонент моторных топлив, растворитель … Естествознание. Энциклопедический словарь
Этилбензол — C6H5CH2CH3, бесцветная жидкость; tkип 136,2°С, tпл 94,97°С, плотность 0,867 г/см3 (20°С); почти нерастворим в воде, растворяется в спирте, бензоле, эфире, четыреххлористом углероде. Э. содержится в нефти и каменноугольной смоле.… … Большая советская энциклопедия
ЭТИЛБЕНЗОЛ — С 6 Н 5 СН 2 СН 3, мол. м. 106,16; бесцв. жидкость с запахом бензола; т. пл. 94,97 … Химическая энциклопедия
ЭТИЛБЕНЗОЛ — C6H5C2H5 бесцветная жидкость; tкип 136,2 °С. Сырьё в синтезе стирола, добавка к моторному топливу, повышающая его октановое число … Большой энциклопедический политехнический словарь
этилбензол — органическое соединение, углеводород ароматического ряда; бесцветная жидкость; содержится в нефти и коксовом газе; в промышленности получают синтетически (из бензола и этилена); примен. для производства стирола и как добавка к моторному топливу.… … Словарь иностранных слов русского языка
Этилбензол
Химическая формула этилбензола
Свойства этилбензола
| Физические свойства | |
|---|---|
| Молярная масса | 106.167 г/моль |
| Плотность | 0.8665 г/см³ |
| Энергия ионизации | 8,76 ± 0,01 эВ |
| Термические свойства | |
| Температура плавления | -95 °C |
| Температура кипения | 136 °C |
| Температура вспышки | 55 ± 1 ℉ |
| Пределы взрываемости | 0,8 ± 0,1 об.% |
| Теплопроводность | 1,726 Вт/(м·K) |
| Давление пара | 7 ± 1 мм рт.ст. |
| Химические свойства | |
| Растворимость в воде | 0.15 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,495 |
Технология производства этилбензола
Наиболее значительные результаты достигнуты в области использования твердых катализаторов, а также совершенствования аппаратурного оформления процессов с применением цеолитных катализаторов. В России же подобные процессы получения этилбензола на твердых катализаторах находятся в стадии разработки.
Схема технологии «EBmax».
В реакторе реагенты находятся в жидкой фазе, катализатор засыпан несколькими слоями, между которыми дополнительно вводится этилен. Конверсия этилена в процессе достигает 100%. Тепло, которое образуется в ходе реакции, отводится на подогрев сырья и получение пара.
Продукты реакций алкилирования и трансалкилирования направлятся в зону разделения, которая состоит из трех ректификационных колонн. Отделяемый бензол направляется в реакторы алкилирования и трансалкилирования, а тяжелый остаток обычно используется в качестве топлива.
Более интересно гомогенное алкилирование в присутствии хлорида алюминия в процессе «Lummus Crest, Inc.», при котором количество катализатора определяется его растворимостью в бензоле, а давление процесса подбирается таким, чтобы олефин находился в жидкой фазе. Реактор работает в адиабатическом режиме, а температура на выходе из него достигает 200 °С. При этом резко уменьшается выход побочных продуктов, а выход этилбензола становится близок к стехиометрическому.
Реактор алкилирования бензола этиленом высшими олефинами на HF-катализаторе представляет из себя колонну, оснащенную ситчатыми тарелками, которые обеспечивают хорошее смешение фаз. Для того чтобы НF-кислота оставалась в жидком состоянии, смесь в реакторе находится под давлением не менее 0,4-0,6 МПа.
Схема реактора алкилирования бензола высшими олефинами
Реакционная смесь с верха реактора выводится в отстойник, в котором производится сепарация НF-кислоты от углеводородов. В процессе алкилирования бензола моноолефинами на цеолитных катализаторах возможно использование как секционированного реактора так и трубчатого реактора.
Реактор алкилирования бензола и изобутана олефинами на цеолитном катализаторе:
Секционирование реактора позволяет иметь высокое отношение бензол: олефины или изобутан: олефины в каждой секции при низком общем их соотношении в процессе, а также состав продуктов, близкий к получаемому на действующих промышленных установках.
В достоинства аппаратов такого типа входят: простота конструкции; непрерывная передача тепла от одного теплоносителя к другому; интенсивный теплообмен. Имеются также и недостатки: металлоемкость; температурные деформации; сложность разборки и чистки трубного пространства. Трубчатые реакторы позволяют эффективно регулировать температуру процесса, что существенно увеличивает селективность, продолжительность работы катализатора, а также выход целевых продуктов
Кислотные катализаторы алкилирования
AlCl3 + 3H2O = Al(OH)3↓ + 3HCl.
Образовавшаяся гидроокись алюминия является малорастворимой, в результате чего забивает аппараты и трубопроводы на производстве, поэтому содержание влаги в бензоле, подаваемом на алкилирование должно быть не более 0,006 %. Перспективным решением существующих технологических проблем и недостатков в процессах алкилирования ароматических углеводородов является переход на гетерогенные цеолитсодержащие катализаторы.
Цеолитные катализаторы
В сравнении с кислотными катализаторами цеолитные катализаторы имеют ряд преимуществ:
достаточно устойчивы к примесям в сырье;
проявляют большую активность и селективность в процессе;
отсутствуют проблемы с коррозией и экологией;
упрощается технологическое оформление процесса.
Для процесса алкилирования бензола и трансалкилирования ди- и полиалкилбензолов цеолитсодержащие катализаторы впервые начали разрабатывать с середины 60-х годов прошлого века. В 1976 году компанией Mobil-badger была пущена первая газофазная установка с применением катализаторов на основе цеолита типа ZSM-5. После успешного внедрения процесса получения этилбензола на цеолитсодержащих катализаторах данная технология быстро заняла лидирующее положение. Ученые с разных стран стали активно разрабатывать различные цеолитные катализаторы, а также совершенствовать процесс. В 2003 году в США разработали способ получения этилбензола в присутствии катализатора, в котором первый пористый неорганический материал представляет собой ZSM-5, а второй пористый неорганический материал является силикалитом 1 или силикалитом 2. Недостатком данных способов алкилирования бензола этиленом является недостаточно высокий выход этилбензола и селективность по целевому продукту. Кроме изобретения новых катализаторов, со времен пуска первой установки получения ЭБ на цеолитных катализаторах, процесс претерпел и ряд технологических изменений и модернизаций:
Проведение алкилирования и последующего трансалкилирования в отдельных реакторах (диэтилбензольная фракция выделяется в блоке фракционирования и в количестве, превышающем термодинамически равновесную концентрацию, подается в реактор трансалкилирования);
Перевод процесса алкилирования и трансалкилирования из области высоких температур, соответствующих жидкофазным условиям.
Разделением процессов алкилирования и трансалкилирования привело к существенному увеличению величины конверсии ди- и полиалкилбензолов, а перевод процесса в жидкую фазу позволило не только снизить температуру процесса и продлить срок службы катализатора, но и повысить выход этилбензола на 10% за счет снижения доли побочных реакций. Однако переход от газофазного оформления процесса к жидкофазному требовал новых катализаторов.
Нецеолитные катализаторы
Катализаторы с микро-мезопористой структурой




СОДЕРЖАНИЕ
Возникновение и приложения
По состоянию на май 2012 года для этой цели используется более 99% всего производимого этилбензола.
Ниша использует
Производство
Промышленные методы
Этилбензол производится в больших масштабах путем объединения бензола и этилена в химической реакции, катализируемой кислотой :
В 2012 году таким способом было произведено более 99% этилбензола. Таким образом, производители этилбензола являются основными покупателями бензола, на их долю приходится более половины от общего объема производства.
Воздействие на здоровье
По состоянию на сентябрь 2007 года Агентство по охране окружающей среды США (EPA) определило, что питьевая вода с концентрацией 30 частей на миллион (ppm) в течение одного дня или 3 ppm в течение десяти дней, как ожидается, не окажет какого-либо неблагоприятного воздействия на детей. Ожидается, что воздействие 0,7 ppm этилбензола в течение всей жизни также не окажет отрицательного воздействия. Управление по безопасности и гигиене труда США (OSHA) ограничивает воздействие на рабочих в среднем 100 ppm в течение 8-часового рабочего дня или 40-часовой рабочей недели.
Этилбензол классифицируется как возможный канцероген Международным агентством по изучению рака (IARC), однако EPA не определило этилбензол как канцероген. Национальная токсикологическая программа провела ингаляционное исследование на крысах и мышах. Воздействие этилбензола привело к увеличению случаев опухолей почек и яичек у самцов крыс и тенденции к увеличению опухолей почек у самок крыс, опухолей легких у самцов мышей и опухолей печени у самок мышей.
Как и все органические соединения, пары этилбензола образуют с воздухом взрывоопасную смесь. При транспортировке этилбензол классифицируется как легковоспламеняющаяся жидкость класса 3, группа упаковки II.
Воздействие на окружающую среду
С 2012 года в соответствии с Директивой ЕС по опасным веществам этилбензол не классифицируется как опасный для окружающей среды.
Биоразложение
Некоторые штаммы грибка Cladophialophora могут расти на этилбензоле. Бактерия Aromatoleum aromaticum EbN1 была обнаружена благодаря ее способности расти на этилбензоле.
Что такое стирол? состав, свойства, применение
Стирол в основном используется для производства термопластичного полимера под названием полистирол, а также ряда других пластмасс и синтетических каучуков. Этот легкий и недорогой материал обеспечивает высококачественный внешний вид, который можно разрезать на любую форму.
Профиль стирола
Стирол является членом углеводородной винильной группы (CH2=CH-), молекулы которой состоят из двойной связи между двумя атомами углерода.
Под действием инициаторов и катализаторов эта двойная связь может расщепляться на две одинарные связи, связывающие атом углерода другой молекулы стирола. Так образуется полистирол, в котором тысячи соединений стирола прикреплены вдоль углеродной основы.
Физические и химические свойства
Стирол представляет собой бесцветную маслянистую жидкость, которая легко испаряется. Старый образец может выглядеть слегка желтоватым. Хотя он имеет сладковатый запах, другие химические вещества могут придать ему резкий, неприятный привкус.
Хотя стирол плохо растворяется в воде, он хорошо растворяется в этаноле, эфире и ацетоне и слабо растворяется в четыреххлористом углероде. Также он образует однородную смесь с бензолом.
Стирол менее плотен, чем вода, но его пары тяжелее воздуха и раздражают глаза. Если он полимеризуется в закрытом контейнере, контейнер может разорваться на части.
Вязкость: 0,696 сП при 25 °C
Полимеризация: Постепенно при комнатной температуре и легко при температуре выше 65 °C.
Полимеризация также может происходить из-за присутствия пероксидов, окислителей или солнечного света. Чтобы предотвратить это, стирол обычно смешивают с ингибиторами. Однако это не препятствует стиролу разъедать медь и медные сплавы.
Как производится стирол?
Натуральный стирол содержится (в очень небольших количествах) в некоторых продуктах и растениях, таких как кофейные зерна, арахис, корица и бальзамические деревья. Он также содержится в каменноугольной смоле.
В настоящее время для производства стирола из этилбензола используются два процесса:
1. Дегидрирование этилбензола.
Около 75% стирола получают путем удаления водорода из этилбензола (C 6 H 5 CH 2 CH). Этот процесс включает нагревание этилбензола до 600 °C в присутствии катализатора, которым обычно является оксид железа (III).
Реакция поглощает значительное количество тепла (из внешней среды) и является обратимой. При этом выделяется 88-94% стирола, который затем очищается путем дистилляции.
Поскольку во время процесса стирол может подвергаться термической полимеризации, в систему постоянно добавляют ингибитор.
2. Обработка этилбензола кислородом
Реакция между этилбензолом и кислородом дает гидропероксид этилбензола. Затем этот продукт обрабатывают пропиленом для получения оксида пропилена и 1-фенилэтанола. Наконец, дегидратация 1-фенилэтанола дает стирол.
Более дешевая альтернатива
Стирол также можно получить, используя недорогое сырье: метанол (простейший спирт) и толуол (ароматический углеводород).
Реакция между этими соединениями при 425 °C и в присутствии цеолитного катализатора дает смесь стирола и этилбензола 9:1. Выход стирола более 60%.
Из коричной кислоты
Обычное использование
Ежегодно миллиарды килограммов стирола производятся промышленным способом для изготовления таких продуктов, как пищевые контейнеры, одноразовые стаканчики, пластик, резина, трубы, стекловолокно, автомобильные компоненты и различные химикаты.
Хотя стирол в основном используется для производства полистирольных пластиков и смол, он также служит промежуточным звеном в синтезе соединений, используемых для ионообменных смол.
В частности, стирол используется для производства:
Твердый полистирол, из которого делают жесткую тару для предприятий общественного питания, кухонную технику, игрушки, медицинские и оптические инструменты.
Полимерные композиты, армированные волокном, которые используются для производства коррозионно-стойких труб и резервуаров, спортивных товаров, компонентов ветряных турбин, военных и коммерческих самолетов и автомобильных запчастей.
Пенополистирол и пленки, которые используются для изготовления контейнеров для предприятий общественного питания, легкой защитной упаковки, а также для ламинирования и печати.
Самыми популярными материалами на основе стирола являются:
Токсичность
Стирол представляет опасность при хранении при температуре выше 32 °C. При разложении (при нагревании) он выделяет едкий дым и раздражающие испарения.
Пары стирола сильно раздражают горло, нос, глаза и легкие. У работников, подвергающихся воздействию высоких уровней паров стирола, могут развиться дегенеративные заболевания нервной системы.
Длительное воздействие может привести к усталости, потере слуха, ухудшению цветового зрения, снижению концентрации, замедлению реакции и психическим проблемам. У некоторых работников наблюдались астма, аллергические кожные реакции, изменения иммунной функции и даже свертываемость крови.
Размер рынка
В 2019 году мировой рынок стирола оценивался в 48 миллиардов долларов. Прогнозируется, что к 2026 году эта цифра достигнет 70 миллиардов долларов при среднегодовом темпе роста (CAGR) в 4,6% с 2020 по 2026 год.
Однако растущие проблемы со здоровьем и окружающей средой при использовании стирола будут тормозить рост рынка. За последнее десятилетие были зарегистрированы различные промышленные аварии. Недавно, в мае 2020 года, в результате утечки газообразного стирола погибли тринадцать рабочих на заводе LG Chem в Висакхапатнаме, Индия.
Несмотря на вредные последствия, стирол будет пользоваться значительным спросом благодаря применению полистирола. Азиатские страны будут продолжать доминировать на рынке в течение прогнозного периода.
В частности, ожидается, что в Китае в ближайшие годы будет наблюдаться устойчивый рост из-за растущего спроса на упакованные товары в продовольственном сегменте.
Часто задаваемые вопросы
Как люди подвергаются воздействию стирола?
Стирол может попасть в организм человека при дыхании (в виде пара) или при прямом контакте с кожей. Население в целом может подвергаться воздействию при употреблении питьевой воды, употребления пищи, курения сигарет, вдыхания воздуха в помещении или использования потребительских товаров, содержащих стирол.
При попадании в окружающую среду стирол попадает в воздух с поверхности воды и влажной почвы. Небольшие количества стирола были обнаружены как в организмах, дышащих воздухом (морские птицы, хищники, люди), так и в организмах, дышащих водой (хищные рыбы).
Насколько опасен стирол?
Оксид стирола может быть канцерогенным как для человека, так и для животных. У животных он вызывает рак печени. Безопасного уровня воздействия этого газа не существует, поэтому любой контакт с ним должен быть сведен к минимально возможному уровню.
Как быстро стирол попадает в организм?
Во многих контролируемых исследованиях было установлено, что стирол задерживается в легких до 70% от вдыхаемой дозы. В окружающем воздухе он может абсорбироваться через кожу на уровне 4% от дозы, поглощенной в дыхательных путях. Более того, жидкий стирол может проникать через кожу со скоростью 1 мкг/м2 в минуту.
Как защитить себя от газообразного стирола?
Работники могут использовать средства защиты и следовать аварийным процедурам, чтобы обезопасить себя. Это включает обеспечение достаточной вентиляции и устранение всех источников воспламенения на предприятии.
Не допускайте скопления паров в небольших помещениях и предотвращайте любые утечки или проливы. Также необходимо избегать выброса продукта в окружающую среду.




Этилбензол является органическое соединение с формулой C6ЧАС5CH2CH3. Это легковоспламеняющаяся бесцветная жидкость с запахом, аналогичным запаху бензин. Этот моноциклический ароматный углеводород важно в нефтехимическая промышленность в качестве промежуточного звена в производстве стирол, предшественник полистирол, обычный пластик материал. В 2012 году более 99% произведенного этилбензола было израсходовано на производство стирола.
Содержание
Возникновение и приложения
Этилбензол встречается в природе в каменноугольная смола и нефть. [4]
По состоянию на май 2012 г. для этой цели используется более 99% всего производимого этилбензола.
Ниша использует
Этилбензол добавляют в бензин в качестве антидетонационный агент для уменьшения детонации двигателя и повышения октанового числа. Этилбензол часто встречается в других промышленных продуктах, включая пестициды, ацетат целлюлозы, синтетическая резина, краски и чернила. [4] Используемый при добыче природного газа, этилбензол можно закачивать в землю.
Производство
Этилбензол производится в больших масштабах путем сочетания бензол и этилен в кислотно-катализируемом химическая реакция. В 1999 году было произведено около 24 700 000 тонн. [5]
Промышленные методы
Этилбензол производится в больших масштабах путем сочетания бензол и этилен в кислотно-катализируемом химическая реакция:
В 2012 году таким способом было произведено более 99% этилбензола. Таким образом, производители этилбензола являются основными покупателями бензола, на их долю приходится более половины от общего объема производства. [6]
Небольшие количества этилбензола извлекаются из смеси ксилолы суперфракционированием расширение дистилляция процесс. [7]
В 1980-х годах процесс на основе цеолита с использованием парофазного алкилирования обеспечивал более высокую чистоту и выход. Затем был введен жидкофазный процесс с использованием цеолит катализаторы. Это обеспечивает низкое соотношение бензола и этилена, уменьшая размер необходимого оборудования и уменьшая производство побочных продуктов. [8]
Влияние на здоровье
Острый токсичность этилбензола низкое, с LD50 около 4 граммов на килограмм массы тела. Долгосрочная токсичность и канцерогенность неоднозначно. [5] Чувствительность глаз и горла может возникнуть при воздействии высокого уровня этилбензола в воздухе. При более высоком уровне воздействия этилбензол может вызвать головокружение. [4] Попадая в организм, этилбензол биоразлагается до 1-фенилэтанола, ацетофенон, фенилглиоксиловая кислота, миндальная кислота, бензойная кислота и гиппуровая кислота. [5] Воздействие этилбензола можно определить путем тестирования продуктов распада в моча.
По состоянию на сентябрь 2007 г. Агентство по охране окружающей среды (EPA) определили, что питьевая вода с концентрацией 30 частей на миллион (ppm) в течение одного дня или 3 ppm в течение десяти дней, как ожидается, не окажет какого-либо неблагоприятного воздействия на детей. Ожидается, что воздействие 0,7 ppm этилбензола в течение всей жизни также не окажет отрицательного воздействия. Соединенные штаты. Управление по охране труда (OSHA) ограничивает воздействие на рабочих в среднем до 100 частей на миллион в течение 8-часового рабочего дня и 40-часовой рабочей недели. [4]
Этилбензол классифицируется как возможный канцероген Международное агентство по изучению рака (IARC), однако EPA не определило этилбензол как канцероген. Национальная токсикологическая программа провела ингаляционное исследование на крысах и мышах. Воздействие этилбензола привело к увеличению случаев опухолей почек и яичек у самцов крыс и тенденции к увеличению опухолей почек у самок крыс, опухолей легких у самцов мышей и опухолей печени у самок мышей.
Как и все органические соединения, пары этилбензола образуют с воздухом взрывоопасную смесь. [7] При транспортировке этилбензол классифицируется как легковоспламеняющаяся жидкость 3 класса, Группа упаковки II. [7]
Экологические последствия
Этилбензол содержится в основном в виде пара в воздухе, поскольку он может легко перемещаться из воды и почвы. [4] Средняя концентрация 0,62 частей на миллиард (ppb) был обнаружен в городском воздухе в 1999 году. [9] Исследование, проведенное в 2012 году, показало, что в воздухе страны средняя концентрация составила 0,01 частей на миллиард, а в помещении средняя концентрация составила 1,0 частей на миллиард. Он также может выбрасываться в воздух при горении каменный уголь, газ и масло. Использование этилбензола в промышленности способствует образованию паров этилбензола в воздухе. После трех дней пребывания в воздухе под воздействием солнечного света другие химические вещества расщепляют этилбензол на химические вещества, которые можно найти в смог. [4] Поскольку он плохо связывается с почвой, он также может легко перемещаться в грунтовые воды. В Поверхность воды, он разрушается, когда вступает в реакцию с химическими веществами, которые естественным образом содержатся в воде. [10] Как правило, этилбензол не содержится в питьевой воде, однако его можно найти в колодцах с питьевой водой в жилых помещениях, если колодцы расположены рядом с свалками отходов, протекающими подземными резервуарами для хранения топлива или свалками. [4]
С 2012 года в соответствии с Директивой ЕС по опасным веществам этилбензол не классифицируется как опасный для окружающей среды. [7]
Этилбензол входит в состав табачный дым. [11]
Биоразложение
Некоторые штаммы гриба Кладофиалофора может расти на этилбензоле. [12] Бактерия Aromatoleum aromaticum EbN1 был открыт благодаря его способности расти на этилбензоле. [13]