что способствует выработке гормона роста
Как “догнать” рост?
Известно, что одной из характеристик физического развития детей и подростков является рост. “Можно ли как-то повлиять на рост?” — часто спрашивают заботливые родители. На этот и другие вопросы отвечает Елена ЛОБЫКИНА, доктор медицинских наук, профессор, врач-диетолог ГБУЗ КО “Новокузнецкий центр медицинской профилактики”:
— Для ответа на этот вопрос немного напомню, как рост происходит. В течение жизни ребенка, до момента достижения окончательного роста, идет смена периодов ускоренного и замедленного роста. Формирование костей заканчивается в среднем к 25 годам. К этому возрасту происходит формирование так называемого “пика костной массы”, когда происходят ускорение линейного роста, интенсивное нарастание костной массы и увеличение размеров кости. Выделяют три периода наибольшего скачка роста: первый год жизни (рост увеличивается на 50% от длины тела при рождении); 5-6 лет и 13-15 лет (пубертатный скачок роста). Участвуют в процессах роста практически все гормоны, особенно это относится к гипофизу, щитовидной железе и половым железам (особенно в период пубертата). В связи с этим при задержке роста необходимо исключить заболевания этих эндокринных органов.
— Какие факторы способствуют замедлению роста ребенка?
— На рост влияют наследственность, конституциональные особенности и наличие заболеваний. Дефицит гормона роста встречается редко, чаще встречаются конституциональные особенности роста (особенно у мальчиков). Плохо растут дети невысоких родителей с так называемым “семейным замедленным созреванием”. Задержка роста и пубертата могут наблюдаться как при резком дефиците массы тела в результате недостаточной калорийности или несбалансированного питания (нервная анорексия, попытка похудеть на низкокалорийных диетах), так и при ожирении у подростков. Главный ориентир, на который надо обратить внимание при исключении гормональной проблемы задержки роста (дефицита гормона роста), — это отсутствие динамики роста ребенка в течение года.
— Может ли питание влиять на рост ребенка?
— Да, может. Для поддержания концентрации и ритма секреции гормона роста полноценное и сбалансированное питание (достаточное количество и правильный баланс не только белков, жиров и углеводов, но и витаминов и минеральных веществ) крайне необходимо. Это достаточно частая причина отставания в росте у детей.
В первые годы жизни задержка роста может возникнуть из-за недостаточности питания, нарушения кишечного всасывания. Если ребенок с раннего детства отстает в росте от сверстников, а причина отставания неясна, необходимо обязательно исключить скрытое течение у ребенка целиакии — заболевания, сопровождающегося непереносимостью глютена (клейковины) — белка, который содержится в пшенице и некоторых других злаках. Нарушения функции кишечника приводят к развитию всасывания необходимых пищевых веществ.
— Как естественным путем, с помощью питания, повысить секрецию гормона роста?
— Доказано, что белково-энергетическое недоедание, дефицит в питании витаминов (А, Д) и минеральных веществ (кальция, железа, йода, цинка и др.) приводят к нарушению роста. Белок необходим для правильного формирования костной и хрящевой ткани, а также для образования гормонов, регулирующих рост, в том числе и самого гормона роста. Соответственно, недостаток белка в пище напрямую может влиять на задержку роста. Кроме того, дефицит полноценного белка нарушает процессы всасывания витаминов и минеральных веществ из пищи. Дефицит белка может проявляться у детей снижением мышечной массы (в том числе и массы тела) и болью в мышцах, линейной деформацией костей, изменениями со стороны кожи (изменение цвета, сухая шелушащаяся кожа, длительно не заживающие язвы и раны).
— Как на рост влияет витамин D?
— Витамин D за счет регуляции фосфора и кальция и повышения всасывания кальция в кишечнике регулирует костный обмен, предупреждая развитие рахита и остеопороза. Пищевые источники — это печень животных, желток яиц, молоко, масло, сметана, икра. Профилактика дефицита витамина D может быть достигнута путем увеличения солнечного облучения, употребления продуктов, богатых витамином D, и ежедневного приема витамина D. У нас принято активное назначение витамина D детям до 1-2 лет с целью профилактики рахита, затем про витамин D “забывают”, особенно в подростковом возрасте. Между тем в нашей стране среди всех групп населения наблюдается дефицит витамина D различной степени, что требует при ликвидации дефицита подключения лечебных доз, и не в режиме курсового, а более длительного его применения.
— Можно ли передозировать витамин D?
— Получить передозировку можно, если без исследования крови, например, назначить высокие взрослые лечебные дозы витамина D маленькому ребенку. В реальной практике у детей и подростков получить передозировку трудно, если только не принимать месяц по бутыльку капель витамина в неделю. Это крайности. Уж слишком дефицитен витамин D в питании россиян любого, в том числе детского и подросткового возраста. Поэтому вышеуказанные дозировки являются минимальными профилактическими дозами. Наоборот, чаще должен возникать вопрос: “А достаточна ли для моего ребенка эта доза?”
— Что еще поможет “догнать” рост?
— Для образования гормона роста необходим цинк, который стимулирует образование и минерализацию костной ткани, участвует в образовании ферментов, регулирующих рост и обмен белка. Около 30% всего содержащегося в организме цинка находится в костях. Основной источник цинка — мясные продукты. Помимо этого, к продуктам, богатым цинком, относятся тыква, семена кабачков, мясо краба, арахис.
К сожалению, Западная Сибирь относится к регионам не только дефицитным по йоду, но и железу. Отмечают, что латентный (скрытый) железодефицит может встречаться у 50 — 60% подростков. Логично полагать, что питание и дыхание любой клетки, тем более растущей, как кость, будет нуждаться в хороших дотациях железа. Кроме этого, гипоксия, развивающаяся при дефиците железа, будет влиять и на синтез гормона роста.
Контролируют линейный рост (особенно в первые годы жизни ребенка) и гормоны щитовидной железы, для образования которых необходим йод и животный белок. Напомню, что идеальной комбинацией этого являются морская рыба и морская капуста. Гораздо меньше йода содержится в нашем традиционном (“безрыбном”) рационе питания. Не забывайте про любую возможность включать в рацион обогащенные йодом продукты питания (например, соль и хлеб). В организме все очень взаимосвязано.
Таким образом, только разнообразное, не однотипное изо дня в день, питание, с включением всех групп продуктов, может улучшить ростовые показатели ребенка и подростка.
— Какие еще факторы, кроме питания, могут влиять на рост?
— Для нормального роста ребенка также важны: качество и продолжительность сна. Увеличение продолжительности сна способствует увеличению выделения гормона роста. Подросткам в этот период спать желательно 8-10 часов. Помимо сна регулярная физическая аэробная нагрузка: занятия плаванием, гимнастикой (турник), легкой атлетикой. Анаэробные физические упражнения (марафоны, тяжелая атлетика) могут привести к задержке темпов и в конечном счете к достижению небольшого конечного роста.
Соматотропин – гормон роста и «гормон молодости». Почему он важен и зачем нужны анализы
Человеческий гипофиз вырабатывает разные химические соединения – гормоны, регулирующие развитие организма, обмен веществ и работу желез внутренней секреции. Один из таких гормонов – соматотропин (или соматропин, СТГ). Нормальный уровень этого вещества крайне важен для детей и подростков, а также для спортсменов и женщин – особенно тех, кто желает подольше сохранить молодость организма. Что это за гормон, какова его роль в организме и где можно сдать анализы на него – читайте в нашей статье.
Соматотропный гормон участвует во множестве органических процессов – обмене веществ (белков, жиров, углеводов), регуляции водного баланса, а также он напрямую связан с ростом организма. Именно поэтому пик его концентрации в организме приходится на детский возраст, когда ребенок интенсивно растет. Если же в организме малыша недостаточно гормона роста – он будет отставать по этому параметру от своих сверстников, а иногда дефицит соматропина может даже вызывать проблемы в общем развитии.
ВАЖНО! Избыток гормона роста в организме ребенка тоже может приводить к неприятностям – в данном случае рост организма будет происходить гораздо интенсивней, чем это необходимо по норме. Человек с избытком соматотропина обычно продолжает расти и после окончания полового созревания, что может привести к гигантизму и/или акромегалии – патологическим отклонениям, значительно ухудшающим качество жизни.
Итак, максимально активно гормон роста вырабатывается в период от рождения до конца полового созревания. Однако нормальный уровень соматотропина крайне важен и для взрослых людей, ведь без него невозможны нормальные процессы формирования костной ткани, поддержка тонуса мышц, правильный метаболизм.
Почему гормон роста также называют «гормоном молодости»
Согласно результатам некоторых исследований, соматотропин способен омолаживать организм – как внешне, так и изнутри. Первый эксперимент, касающийся этого свойства гормона роста, был проведен еще в 80-х годах прошлого века иммунологом Грегори Фейхи. В результате было установлено, что соматропин может омолаживать клетки организма, буквально «поворачивая время вспять».
ВАЖНО! Гормон роста имеет и негативный побочный эффект – он может способствовать разрастанию уже имеющихся в организме опухолей (как доброкачественных, так и злокачественных). Поэтому, если анализ на соматотропин показывает его повышенный уровень – рекомендуется пройти медицинское обследование на наличие опухолей.
Откуда получать соматотропин при его недостатке?
Уровень этого гормона колеблется в зависимости от времени суток. Самая высокая его концентрация в организме – во время сна. А это значит, что для поддержки нормальной выработки соматотропина нужно полноценно высыпаться, причем ложиться спать нужно не позже 22:00.
Повышают уровень соматотропина и умеренные физические нагрузки. А чтобы выработка гормона не «затухала» подольше, нельзя отказываться от животного белка в пище (мясо, рыба). Дело в том, что секреция соматотропина усиливается «в ответ» на присутствие особых аминокислот, которые содержатся в белке.
Посоветовавшись с врачом, также можно начать прием соматотропина в виде таблеток или инъекций. Препараты на основе гормона роста продаются не только в аптеках, но и в магазинах для спортсменов.
Между прочим, усилить выработку организмом гормона роста можно и с помощью приема некоторых аминокислот, а именно – орнитина, аргинина, глутамина и лизина. Принимать их необходимо натощак, непосредственно перед сном.
Где можно сдать анализ на гормон роста
Все взрослые и маленькие пациенты могут пройти исследование крови на содержание соматотропина в отделениях всеукраинской сети лабораторий «МедЛаб».
Показания к проведению этого анализа включают в себя:
Чтобы результаты анализа были максимально точными, придерживайтесь следующих правил подготовки к его сдаче:
ВАЖНО! В течение 24 часов до анализа следует исключить прием любых лекарственных препаратов, витаминов и БАДов, а если это невозможно – обязательно предупредить лечащего врача.
Например, глюкоза, глюкокортикоиды, прогестерон снижают уровень СТГ в крови, а леводопа, L-триптофан, диазепам, эстрогены – повышают. Разумеется, приведенный список неполный – влиять на уровень СТГ могут очень многие препараты и помимо перечисленных.
Роль гормона роста в регуляции жирового и углеводного обмена
Исследования, проводимые в последнее время и посвященные изучению различных факторов, участвующих в развитии ожирения, наглядно демонстрируют: гормон роста (ГР) играет активную роль в регуляции основного обмена.
Исследования, проводимые в последнее время и посвященные изучению различных факторов, участвующих в развитии ожирения, наглядно демонстрируют: гормон роста (ГР) играет активную роль в регуляции основного обмена. До сих пор не совсем понятно, почему при двух противоположных состояниях (акромегалии — состоянии, сопровождающемся повышенной секрецией ГР, и соматотропной недостаточности) имеют место схожие нарушения обмена: развитие ожирения, сахарный диабет, гиперлипидемии и дислипопротеидемии.
Говоря о метаболических эффектах гормона роста, необходимо помнить о том, что ГР не только является анаболическим гормоном, но также обладает антинатрийуретической и липолитической активностью. Ростовые факторы (ИФР-1, ИФР-2), помимо того что через них действует ГР, оказывают и собственное воздействие на органы и ткани организма. Большая часть циркулирующего в крови ИФР-1 продуцируется печенью, последний может синтезироваться в ряде органов и тканей, где действует как ауто- и/или паракринный ростовой фактор.
Об участии ГР в развитии и функционировании иммунной и кроветворной систем известно достаточно давно. Практически все клетки, относящиеся к системе лимфогемопоэза, не только имеют функционально активные рецепторы к ГР и ИФР-1 (Tapson et al., 1988; Johnson et al., 1992), но и синтезируют указанные соединения. Примером воздействия соматотропина на иммунокомпетентные клетки можно считать тот факт, что введение ГР гипофизэктомированным крысам восстанавливало клеточный и гуморальный иммунитет и повышало выживаемость гипофизэктомированных крыс, инфицированных Salmonella tiphy, в той же степени, что и тетрациклин (Еdvards et al., 1991).
ГР стимулирует синтез и секрецию ИФР-1 в печени, ИФР-1, в свою очередь, по механизму отрицательной обратной связи регулирует секрецию ГР. Большая часть ростовых факторов, синтезируемых в печени, находится под контролем не только ГР, но и инсулина. Так, снижение уровня инсулина, наблюдаемое у пациентов с сахарным диабетом первого типа, сочетается с уменьшением в крови уровня циркулирующего ИФР-1 и увеличением концентрации ГР.
Среди многочисленных факторов, влияющих на энергетический обмен, наиболее пристальное внимание клиницистов и исследователей в последнее время привлекает лептин, вырабатывающийся адипоцитами белой жировой ткани. Он выступает как антагонист нейропептида Y, синтезируемого аркуатным ядром гипоталамуса, в результате формируется ось, направленная на стимуляцию и торможение чувства насыщения: лептин усиливает чувство насыщения, нейропептид Y стимулирует чувство голода. Установлена прямая зависимость между концентрацией лептина и ИМТ, а также процентом жировой массы.
Достаточно интересен механизм взаимодействия между лептином и основными соединениями, принимающими активное участие в энергетическом обмене. Концентрация лептина у женщин в несколько раз превосходит таковую у мужчин, что может быть связано с преобладанием подкожно-жировой клетчатки над висцеральной у женщин, а также с положительным влиянием, оказываемым эстрогенами на концентрацию лептина. Предполагается, что именно лептин служит у женщин маркером достижения критической жировой массы, необходимой для наступления менархе и запуска репродуктивной функции.
Достаточно интересен механизм взаимодействия лептина и инсулина: в ответ на повышение инсулинемии адипоциты активизируются, что ведет к повышению концентрации лептина. В свою очередь, лептин, воздействуя на собственные рецепторы, локализованные на поверхности β-клеток, тормозит выброс инсулина. Однако данные, полученные Dagogo- Gack S., опровергают наличие корреляции между гиперлептинемией и гиперинсулинемией, в связи с чем принципы взаимодействия между лептином и инсулином требуют дальнейшего уточнения и изучения.
Хорошо известно, что гиперсекреция ГР вызывает многочисленные нарушения в функционировании органов и систем организма. Стимулируя рост мягких тканей, ГР способствует значительному увеличению размеров сердца. При этом диаметр клапанного аппарата остается прежним. В результате формируется недостаточность кровообращения. Обладая диабетогенными свойствами, ГР в высоких концентрациях приводит к стимуляции гликогенолиза, торможению утилизации глюкозы мышцами, повышает активность инсулиназы печени. Повышенная концентрация свободных жирных кислот вследствие активации липолиза угнетает активность гликолитических ферментов в периферических тканях и затрудняет утилизацию глюкозы периферическими тканями. Эти нарушения способствуют формированию инсулинорезистентности в 50-60% случаев и, вероятно, могут приводить к развитию сахарного диабета второго типа — в 20% случаев. Развитие апноэ во сне в связи с гипертрофией мягких тканей гортани и сужением верхних дыхательных путей повышает риск внезапной смерти у пациентов с акромегалией в три раза (в сравнении с контрольной группой). Не менее серьезным осложнением акромегалии являются разнообразные нарушения деятельности сердечно-сосудистой системы, включающие артериальную гипертензию, увеличение размеров сердца, развитие акромегалической кардиомиопатии и сердечной недостаточности.
Дефицит гормона роста (ДГР) — заболевание, развивающееся в результате тех или иных оперативных, лучевых, механических или иных воздействий на область гипофиза у взрослых и характеризующееся развитием стертой симптоматики. Наиболее характерными признаками ДГР являются снижение качества жизни пациентов, повышение удельного веса жировой с одновременным снижением процента мышечной массы, снижение плотности костной ткани, повышение атерогенности плазмы крови, развитие сердечно-сосудистых осложнений.
ДГР приводит к развитию гиперинсулинемии. Iranmanesh A. с соавторами доказали существование отрицательной связи между ИМТ и периодом полужизни ГР, ИМТ и амплитудой пиков секреции ГР, из чего можно сделать вывод, что, чем ниже концентрация ГР, тем выше показатель ИМТ.
Veldhuis J. D. в 1995 году выявил, что суточная концентрация ГР отрицательно коррелирует с содержанием жировой ткани. Хорошо известно, что развитие алиментарного ожирения сопровождается повышением содержания лептина в сыворотке крови. В условиях развития соматотропной недостаточности лептинемия повышается, что связано с прекращением отрицательного влияния ГР на секрецию лептина адипоцитами. Факт непосредственного воздействия инсулина на гипофиз остается спорным, но, несмотря на малое количество рецепторов к инсулину на поверхности питуитоцитов, торможение секреции и выброса ГР, сопровождающееся снижением концентрации м-РНК и ГР в соматотрофах, было выявлено в экспериментах in vitro.
Декомпенсированная соматотропная недостаточность способствует повышению концентрации ТГ, снижению содержания ЛПВП, повышению уровня фибриногена, активизации ингибитора-1 плазминогенного активатора фибриногена, снижению массы левого желудочка и уменьшению в связи с этим систолического выброса. Все перечисленные факторы способствуют повышению атерогенности плазмы крови, развитию сердечно-сосудистых осложнений у пациентов с дефицитом гормона роста.
Повышение уровня холестерина, липопротеидов низкой плотности (ЛПНП), липопротеидов очень низкой плотности (ЛПОНП), снижение уровня липопротеидов высокой плотности (ЛПВП) зарегистрированы у пациентов с ДГР в сравнении с контрольной группой, подобранной по возрастному и половому принципам. На фоне терапии препаратами гормона роста, проводившейся в ходе семи независимых, слепых, плацебо-контролируемых исследований, организованных в различных клиниках Европы, было продемонстрировано снижение уровня холестерина (выявлено в шести центрах), сочетавшееся со значимым снижением ЛПНП и ЛПОНП. Повышение уровня ЛПВП было зарегистрировано лишь в двух исследовательских центрах. Концентрация триглицеридов и аполипопротеина А за время лечения не изменилась. Отмечалась тенденция к снижению уровня ТГ на фоне терапии ГР у пациентов с повышенным содержанием ТГ до лечения. В ходе другого исследования, проводимого одновременно в шести медицинских центрах, не было отмечено снижения концентрации липопротеина (А) на фоне ЗГТ препаратами гормона роста; в ходе пяти из шести проводимых исследований его концентрация повысилась и не изменилась только в одном.
Два независимых исследования, проведенные в Швеции и Великобритании, были посвящены ретроспективному анализу продолжительности жизни и причинам смерти у пациентов с ДГР. Ретроспективное исследование продолжительности жизни пациентов с подтвержденным диагнозом ДГР позволило выявить более высокий уровень смертности в описываемой группе в сравнении с данными в популяции. Анализ причин смертности позволил достоверно утверждать, что первое место среди них занимают сосудистые заболевания. Два независимых эхокардиографических исследования подтвердили факт достоверного уменьшения массы левого желудочка и снижения систолического выброса у пациентов с ДГР в сравнении с контрольной группой (Rasat R. et al.,1996).
По сравнительным данным, полученным в результате многочисленных исследований, отмечались уменьшение толщины стенки левого желудочка, снижение фракции выброса у пациентов с более чем 20-летним анамнезом дефицита гормона роста (Frustraci A. et al., 1992). Острый инфаркт миокарда, ишемическая болезнь сердца в сочетании с сердечной недостаточностью и цереброваскулярными расстройствами являлись наиболее частыми причинами «сосудистой смерти» у пациентов с ДГР. Заместительная терапия ГР способствовала увеличению толщины стенки левого желудочка, повышению фракции выброса, увеличению массы левого желудочка, повышению ударного объема (Cuneo R. C. et al., 1989).
На принятом в Порт Стефенс консенсусе, посвященном диагностике и лечению ДГР, рекомендовано начинать терапию с низких доз препарата: 0,15-0,30 мг/день или 0,45-0,90 МЕ/день. Для контроля компенсации ДГР используется определение концентрации ИФР-1, именно этот показатель отражает функциональную активность системы гипоталамус-гипофиз-ростовые факторы.
Wiren L. et al. (1998) предлагают следующий расчет дозы препарата: 6 mg /кг/сутки или 0,018 МЕ/кг/сутки, максимальная доза в этом случае не будет превышать 12 mg /кг/сутки или 0,036 МЕ/кг/сутки. В ходе другого исследования нормализация концентрации ИФР-1 наступила при введении средних доз препарата, составляющих 0,6-1,2 МЕ/сутки (Janssen Y. J. H. et al., 1998).
В целях изучения влияния генотропина на показатели липидного обмена и антропометрических показателей у взрослых с ДГР в клинике эндокринологии ММА им. И. М. Сеченова было обследовано 18 пациентов (15 женщин и 3 мужчин) в возрасте 33,5±7 лет с подтвержденным диагнозом ДГР, семь из которых получали генотропин в дозе 1,0±0,2 МЕ/сутки в течение 6 месяцев. Исследовались показатели ИМТ, ОТ/ОБ, ХС, ТГ, ЛПНП, ЛПВП и индекс атерогенности (ИА) до лечения и через 6 месяцев терапии. Все полученные данные сравнивались с аналогичными показателями в группе, не получавшей генотропин. За время лечения в группе, получавшей генотропин, зафиксировано достоверное снижение показателей ОТ (р = 0,02) и ОТ/ОБ (р = 0,04), в отличие от группы сравнения, где рассматриваемые параметры остались прежними — р = 0,9 и р = 0,3 соответственно. В показателях липидного спектра на фоне приема генотропина произошло статистически значимое снижение ХС (р = 0,007), ЛПНП (р = 0,003), ИА (р = 0,003), содержание ТГ не изменилось (р = 0,4), а ЛПВП повысилось (р = 0,002). Среди пациентов, не получавших генотропин, не было отмечено сколь-нибудь значимых изменений в показателях жирового обмена: ХС (р = 0,4), ТГ (р = 0,6), ЛПНП (р = 0,4), ЛПВП (р = 0,3), ИА (р = 0,5). Таким образом, препараты гормона роста эффективно снижают концентрацию ХС, ЛПНП с одновременным повышением содержания ЛПВП, способствуют снижению ОТ и отношения ОТ/ОБ, что уменьшает риск развития висцерального ожирения и сердечно-сосудистых заболеваний у пациентов с ДГР.
Возможности медикаментозной коррекции недостатка гормона роста у взрослых
Каковы основные причины соматотропной недостаточности у взрослых? Каковы ее клинические проявления? Какие методы лабораторно подтверждают диагноз? Как известно, гормон роста (ГР) был последним из классических гормонов, который начали применять с
Каковы основные причины соматотропной недостаточности у взрослых?
Каковы ее клинические проявления?
Какие методы лабораторно подтверждают диагноз?
Как известно, гормон роста (ГР) был последним из классических гормонов, который начали применять с целью заместительной гормональной терапии у взрослых. У детей история медикаментозной коррекции низкорослости насчитывает около тридцати лет, ко взрослым же лечение с использованием биосинтетических препаратов ГР впервые было применено около десяти лет назад. В течение многих лет с целью терапии использовался ГР, получаемый из гипофизарных экстрактов, однако в 1985 году, когда были описаны четыре случая болезни Крейтцфельдта — Якоба у реципиентов гипофизарного ГР, использование последнего было запрещено. Это послужило отправной точкой для начала работ по производству биосинтетического ГР [2].
Использование ГР у детей и произошедший параллельно научный прорыв в отношении диагностирования дефицита гормона роста у взрослых привели к появлению в клинической эндокринологии новой нозологии и, соответственно, новых методов обследования и лечения. Ни один конгресс или симпозиум, проходящий в настоящее время, не обходится без докладов, посвященных проблемам диагностики дефицита ГР (ДГР) у взрослых, выявлению нарушений, сопровождающих заболевание, и принципам подбора терапии.
Для того чтобы создать более точное представление о спектре нарушений, развивающихся на фоне соматотропной недостаточности, необходимо кратко напомнить о структуре ГР, механизмах его секреции и влиянии на органы и системы. ГР, синтезируемый соматотрофами передней доли гипофиза, относится к особому семейству пептидных гормонов, в состав которого кроме ГР входят пролактин (ПРЛ) и плацентарный соматомаммотропин человека (СМЧ). Секреция ГР находится под контролем двух гипоталамических гормонов: соматостатина или соматотропин-ингибирующего фактора (СИФ), который оказывает блокирующее действие на синтез и секрецию соматотрофами ГР. Соматотропин — рилизинг гормон (СРГ) — оказывает стимулирующее действие на соматотрофы, что проявляется увеличением продукции ГР.
Как многие гормоны, ГР синтезируется в определенном импульсном режиме, пики секреции приходятся на 22.00 и 4.00 часа.
Несмотря на существование специфических рецепторов ГР, его действие осуществляется посредством специфических факторов, аналогичных по своей структуре инсулину: инсулиноподобного ростового фактора I (ИФР-I) и инсулиноподобного ростового фактора II (ИФР-II). ИФР-I, действуя через собственные рецепторы, оказывает ростовые эффекты преимущественно в постэмбриональном онтогенезе организма. Действие ИФР-II проявляется преимущественно в процессе эмбриогенеза.
Многочисленные исследования, результаты которых публикуются в современных медицинских изданиях, красноречиво свидетельствуют о наличии серьезных нарушений в соматическом и психологическом статусе пациентов с декомпенсированной недостаточностью гормона роста. Эти нарушения характеризуются изменением соотношения жировая/мышечная ткань в сторону снижения удельного веса последней, увеличения удельного веса жировой ткани и сопровождаются висцеральным отложением последней. При проведении денситометрии обнаруживается снижение плотности костной ткани (МПК). Scacchi at al отметили обратно пропорциональную зависимость между индексом массы тела (ИМТ) и периодом полужизни ГР, а также амплитудой секреции ГР. Процент содержания жировой ткани находился в обратной зависимости от интегрального показателя концентрации ГР, определяемого в течение 24 часов.
Со стороны метаболических нарушений необходимо выделить снижение толерантности к углеводам при проведении инсулинтолерантного теста, увеличение продукции инсулина, проинсулина, повышение содержания триглицеридов плазмы крови, липопротеидов низкой и очень низкой плотности [3].
Не до конца изучено влияние недостаточности ГР на увеличение риска развития сердечно-сосудистых заболеваний, однако при ретроспективном исследовании 333 пациентов с гипопитуитаризмом выявлено, что в течение 22 лет случаи кардиоваскулярной смерти встречались в два раза чаще по сравнению с группой контроля. При проведении эхокардиографии исследователи обнаруживали снижение массы левого желудочка, уменьшение толщины перегородки и задней стенки желудочков, а также снижение фракции выброса левого желудочка.
Еще сравнительно недавно проблема дефицита ГР у взрослых не находила отражения в исследованиях эндокринологов, хотя вопросы, связанные с недостаточностью секреторной функции гипофиза, возникали с того времени, когда были впервые описаны пациентки с синдромом Шиена (Шихана). Данная патология обусловлена развитием инфарктов и кровоизлияний в раннем послеродовом периоде и характеризуется развитием пангипопитуитаризма. Долгие годы пациентки получали заместительную гормональную терапию глюкокортикоидами, тиреоидными гормонами, половыми стероидами, однако при этом продолжали предъявлять неспецифические жалобы на повышенную утомляемость, слабость, немотивированное увеличение массы тела. При попытке исследовать уровень гормонов сыворотки крови с целью выяснения степени компенсации имеющихся нарушений патологических отклонений обнаружено не было, а сниженному уровню ГР не придавали значения. В дальнейшем многочисленные клинические и лабораторные исследования продемонстрировали, что снижение секреции ГР в организме взрослого человека приводит к целому ряду нарушений, которые остаются незамеченными и не имеют такой яркой клинической окраски, как, например, гиперсекреция ГР и развивающаяся вследствие этого акромегалия.
Перечислим причины развития соматотропной недостаточности у взрослых
Количество пациентов, подвергшихся тем или иным вмешательствам на селлярной области, растет год от года, и связано это с повышением разрешающей способности диагностических методов, используемых при обследовании больных, и расширением лечебных возможностей современной медицины. Исходя из этого можно прогнозировать, что количество пациентов, нуждающихся в проведении скринингового обследования ДГР, будет увеличиваться год от года. Современная фармакология, в свою очередь, располагает целым спектром препаратов, призванных компенсировать соматотропную недостаточность; ниже приводится перечень средств, имеющихся на сегодняшний день в отечественной аптечной сети.
«Золотым стандартом» в диагностике ДГР у взрослых справедливо считается инсулинотолерантный тест. Необходимо оговориться, что его проведение возможно только после компенсации вторичного гипотиреоза и вторичного гипокортицизма, в противном случае результаты теста могут быть недостоверными.
В рамках исследования, проведенного в клинике эндокринологии ММА им. И. М. Сеченова и посвященного изучению целесообразности назначения препарата генноинженерного гормона роста взрослым, была обследована группа больных с подозрением на наличие соматотропной недостаточности.
В группу вошли 15 человек в возрасте от 15 до 45 лет: 12 женщин (80%) и трое мужчин (20%). Девять женщин (60%) были прооперированы по поводу макропролактином гипофиза, трое мужчин (20%) и трое женщин (20%) подверглись оперативному вмешательству по поводу краниофарингиомы гипофиза, у одного мужчины (6,7%) при проведении МРТ выявлена агенезия гипофиза. Среди всех обследованных пациентов задержка роста зафиксирована у троих мужчин (20%) в возрасте 16, 21 и 27 лет, оценка роста у них проводилась с использованием таблицы «Перцентильный график роста для мальчиков». У первого пациента рост был равен 148 см, при оценке перцентильных значений величина стандартного отклонения (SDS) составила –3,5. Рост второго и третьего пациентов был равен 145 и 152 см соответственно, но в связи с невозможностью оценить величину SDS исходя из паспортного возраста последняя была рассчитана исходя из костного. В первом случае паспортный возраст ровнялся 13-14 годам и SDS –2, во втором случае костный возраст соответствовал 16 годам и SDS –3. Структура эндокринных заболеваний, выявленных у пациентов с подозрением на соматотропную недостаточность, отражена в табл. 2.
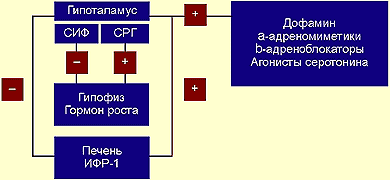 |
| Регуляция секреции гормона роста |
Перед проведением провокационных тестов, направленных на диагностику соматотропной недостаточности, всем пациентам был проведен комплекс лабораторно-диагностических мероприятий для уточнения соматического и гормонального статуса пациентов.
Большинство пациентов получали заместительную гормональную терапию по поводу вторичного гипотиреоза, вторичной надпочечниковой недостаточности, несахарного диабета; у всех было проведено скрининговое исследование концентрации свободного Т4, пролактина, ЛГ, ФСГ, эстрадиола с целью коррекции доз получаемых препаратов.
Исследование соматического статуса предусматривало определение следующих показателей: расчет индекса массы тела (ИМТ), вычисление отношения объем талии/объем бедер (ОТ/ОБ), определение уровня глюкозы, холестерина, триглицеридов, ЛПНП, ЛНВП, АЛТ, АСТ. Проводилось ЭКГ и измерение артериального давления с целью исключения патологии со стороны сердечно-сосудистой системы.
Для оценки качества жизни пациентов с рассматриваемой патологией использовался опросник, разработанный специально для пациентов с дефицитом ГР — QoL-AGHDA (Quality of Life — Assessment of Growth Hormone — Deficiency in Adults) и содержащий 25 вопросов, на которые необходимо было ответить «да» или «нет». Каждый положительный ответ оценивался в один балл; чем больше оказывалась полученная в результате сумма, тем ниже показатель качества жизни.
В ходе обследования были получены следующие результаты.
Нормальные показатели ИМТ (18 30) диагностировано у четырех человек (26,7%). У одного пациента наряду с задержкой роста был выявлен дефицит массы тела, ИМТ составил 15,9 (6,7%). У одной пациентки (6,7%) обнаружен сахарный диабет II типа. Признаки висцерального ожирения выявлены у четырех пациенток (26,7%).
При обследовании у шести пациенток обнаружено повышение гликемии натощак, которое составило 7,025 ± 0,12 ммоль/л; показатели гликемии у 11 пациентов были в пределах нормы и варьировали от 3,6 до 5,5 ммоль/л. Для исключения возможных нарушений углеводного обмена: тощаковой гипергликемии, нарушения толерантности к углеводам, сахарного диабета, гиперинсулинемии всем пациентам был проведен оральный глюкозотолерантный тест с 75 г глюкозы. При определении гликемии через 2 часа после приема 75 г глюкозы последняя составила 6,6 ± 0,14 ммоль/л. Сахарный диабет был выявлен у одной пациентки (гликемия 11,9 ммоль/л), еще у двоих пациентов определено нарушение толерантности к углеводам (гликемия 8,3 и 9,0 ммоль/л). При исследовании уровня С-пептида сыворотки крови были получены следующие результаты: базальная гиперинсулинемия (>2,5 нг/мл) обнаружена у пяти пациентов (3,33%) и составила 3,89 ± 0,1 нг/мл. Более чем двукратное увеличение концентрации С-пептида через 120 минут после стимуляции отмечено у девяти пациентов (60%) и составило 10,5 ± 0,4 нг/мл. При оценке липидного обмена гиперхолестеринемия выявлена у десяти пациентов (66,6%), гипертриглицеридемия обнаружена у семи пациентов (46,6%).
Всем пациентам был проведен инсулинотолерантный тест с целью подтверждения дефицита гормона роста. В условиях стационара пациентам внутривенно вводился инсулин короткого действия: Humulin R или Actrapid HM, из расчета 0,1 ЕД/кг [1]. Исходно через каждые 15 минут в дальнейшем пациентам проводилось определение гликемии в капиллярной крови и забор крови для последующего выявления уровня гормона роста в сыворотке крови.
В ответ на инсулин-индуцированную гипогликемию у 12 обследованных (80%) концентрация ГР не превысила 5 нг/мл, а составила в среднем 0,76 ± 0,013 нг/мл. У троих на фоне гипогликемии было зарегистрировано повышение уровня ГР до 30,78 ± 0,45 нг/мл.
По результатам проведенного теста девяти пациентам была назначена терапия генотропином (Pharmacia&Upjohn). Двое пациентов с задержкой роста получают препарат в настоящее время, у семи человек завершился шестимесячный курс терапии. При расчете дозы препарата использовались рекомендации Janssen и соавт., дозировка генотропина определялась из расчета 0,018 МЕ/кг для шести пациентов, а для трех пациентов с задержкой роста доза была вычислена из расчета 0,1 МЕ/кг [2].
Спустя 6 месяцев после начала терапии все пациенты прошли повторное обследование. Сколько-нибудь значимых изменений ИМТ отмечено не было, показатель ОТ/ОБ снизился у пяти человек, у двоих он остался на прежнем уровне. У троих пациентов выявлено некоторое снижение концентрации холестерина, составившее 8,4, 9,7 и 26,6% от первоначального уровня. У троих пациентов не определено каких-либо изменений, у одного пациента выявлено повышение концентрации холестерина на 17% от исходного. По показателям содержания триглицеридов выявлены следующие данные: у четверых пациентов снижение ТГ составило 56,4, 47,2, 3,7 и 6,3% от исходного. В одном случае динамики отмечено не было, а у двоих человек зафиксировано повышение концентрации ТГ, составившее 68 и 92% от исходного уровня. Снижение уровня ТГ и холестерина на фоне терапии генотропином подтверждается данными зарубежных исследователей, демонстрирующих нормализацию показателей липидного обмена на фоне заместительной терапии.
Перед началом терапии средний показатель качества жизни составил 12,5 балла, а на последней неделе терапии он снизился до 8,9 балла (необходимо отметить, что, по данным Holmes и соавт., у здоровых пациентов, обследованных в Швеции, он составляет 3,7).
Пациент с задержкой роста за 6 месяцев лечения вырос на 5 см, и его рост на момент окончания терапии составил 157 см.
Среди зафиксированных пациентами побочных эффектов чаще всего встречались: отеки, артралгии и миалгии, которые развивались на 3-6-й неделе терапии; о них сообщили четверо пациентов. Аналогичные данные демонстрируют и зарубежные исследователи, проводившие наблюдения за более многочисленными группами пациентов, получавших ГР.
По результатам проведенного исследования можно сделать следующие выводы.
Литература
1. Алгоритмы диагностики и лечения болезней эндокринной системы/ Под ред. И. И. Дедова, 1997.
2. Дедов И. И., Тюльпаков А. Н., Петеркова В. А. Соматотропная недостаточность, 1998.
3. Monson J. P. Growth Hormone Therapy. Oxf, 1999. Р. 93-103.

