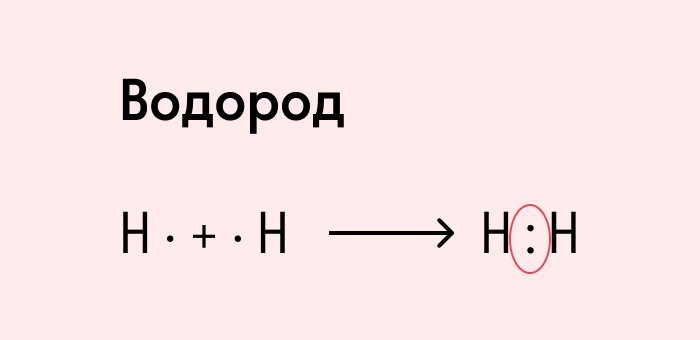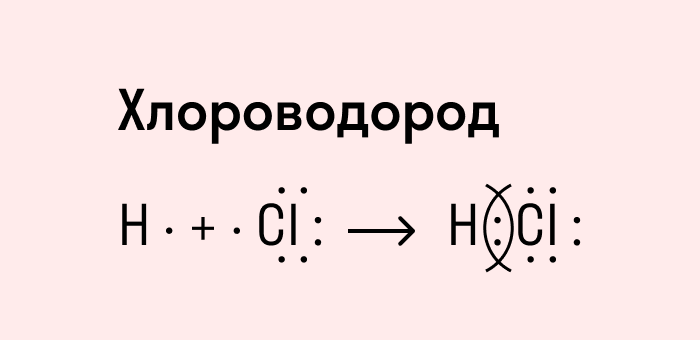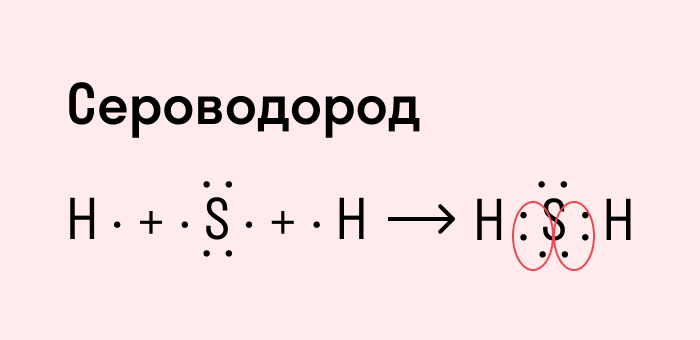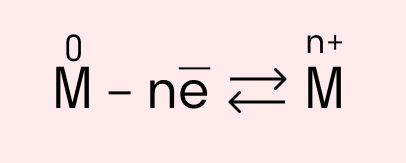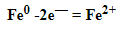Благодаря чему взаимодействуют молекулы 5 букв
Взаимодействие атомов, обусловливающее их соединение в молекулы и кристаллы.
Ответ на вопрос Взаимодействие атомов, обусловливающее их соединение в молекулы и кристаллы., в слове 5 букв:
Связь
Определение слова Связь в словарях
связь — отношение общности, соединения или согласованности.
Например: Солнце в Скорпионе – связь Солнце – Плутон; Плутон в Скорпионе – связь Плутон – Плутон; Меркурий в Скорпионе – связь Меркурий-Плутон; Венера в Скорпионе – связь Венера-Плутон.
Горсовет прирезал к дому участок в двадцать пять соток, три яблони и две буйно плодоносящие груши прикрывали от взоров с улицы грядки с картофелем, Андрюшу впрягали в работу ранней весной, вскапывал землю и отец, гордившийся вековой связью с деревней, в связь эту входили дед его и бабка, уже наученные ублажать огород торфом и навозом.
Впрочем, Маргарет можно лучше всего охарактеризовать, сообщив, что ее единственной связью по расчету была связь с человеком, за которого она вышла замуж в восемнадцать лет, именно тогда она сделала единственное б… заявление, – во всяком случае доказуемое – она сказала Лени: «Я подцепила богатого Кноппа, который во что бы то ни стало хочет на мне жениться».
По существу оба случая могут быть тождественны: устойчивость дневных «остатков» может объясняться установившейся уже во время бодрствования связью их с бессознательными душевными движениями; или же дело происходит несколько сложнее, и не совсем лишенные активности дневные «остатки» только во время сна вступают в связь с вытесненным благодаря облегченному сообщению между Ubw и Vbw.
Беннет (1974) говорит, что путешествия Гурджиева в поисках эзотерического знания, при которых он совершенно свободно пересекал многие великие национальные границы, поддерживались его тайной связью с царским правительством, хотя приписываемая ему связь с Далай-Ламой не подтверждается ни Беннетом, ни другими источниками о Гурджиеве.
Будет ли трудовой связью связь других групп, из которых одна военным путем систематически грабит другую?
Взаимодействие молекул в физике с примерами
Взаимодействие молекул:
Оглядитесь вокруг, и вы увидите множество физических тел. Это и ваш сосед, с которым вы сидите за партой, и сама парта. Это и стул, на котором вы сидите, и ручка, которой вы пишете, и т. п. Все эти тела, как вы уже знаете, состоят из разделенных промежутками частичек, которые постоянно двигаются. Тогда почему частички, из которых состоят физические тела, не разлетаются во все стороны? Более того, тела не только не рассыпаются на отдельные моле кулы — наоборот, чтобы их растянуть, сломать, разорвать, нужно приложить усилие. Попробуем разобраться, почему так.
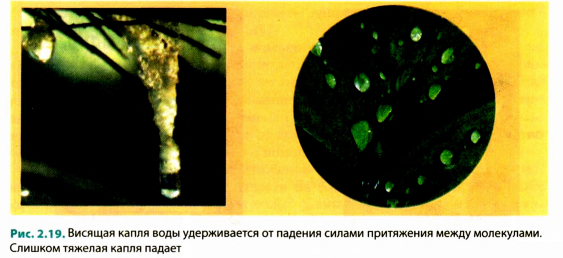
Причина того, что все тела вокруг нас не распадаются на отдельные молекулы, очевидна: молекулы притягиваются друг к другу. Каждая молекула притягивается к соседним молекулам, а те, в свою очередь,— к ней. Именно благодаря межмолекулярному притяжению твердые тела сохраняют свою форму, жидкость собирается в капли (рис. 2.19), скотч прилипает к бумаге, чернила оставляют след на листе, прижатые друг к другу срезами свинцовые цилиндры крепко схватываются (рис. 2.20).
В науке установлено, что притяжение между молекулами действует всегда. Почему же тогда разбитая чашка не становится целой после того, как ее обломки прижмут друг к другу? С какой бы силой мы ни прижимали друг к другу части сломанного карандаша, они также не соединятся в целый карандаш.
Дело в том, что притяжение между молекулами становится заметным только на очень малых расстояниях (таких, которые можно сравнить с размерами самих частичек). Прижимая обломки чашки или части сломанного карандаша, мы приближаем на такие расстояния только очень малое количество молекул. Расстояние же между большинством из них остается таким, что молекулы практически не взаимодействуют. Теперь становится понятным, почему для того, чтобы свинцовые цилиндры слиплись, необходимо предварительно отшлифовать срезы, а кусочки мягкого воска или пластилина легко слипнутся и без всякого шлифования.
Два сухих листа невозможно сблизить настолько, чтобы они соединились. Однако если смочить листы водой, то они слипнутся, так как молекулы воды приблизятся к молекулам бумаги настолько, что межмолекулярное притяжение уже будет удерживать листы друг возле друга (рис. 2.21).
Межмолекулярное притяжение также является причиной смачивания или несмачивания тела определенными жидкостями (рис. 2.22).
Межмолекулярное отталкивание:
Выше мы доказали, что между молекулами существует притяжение. Учитывая это, возникает целый ряд вопросов. Почему же молекулы газов, в беспорядке двигаясь и постоянно сталкиваясь между собой, не слипаются
Рис. 2.22. Капелька воды растекается по поверхности чистого стекла (смачивает ее), поскольку притяжение между молекулами жидкости больше, чем между молекулами жидкости и стекла (о). Притяжение между молекулами воды больше, чем между молекулами воды и жира, которым покрыты перья водоплавающих птиц поэтому вода не смачивает их (вспомните выражение «как с гуся вода») (б) в один большой ком? Почему, если сжать, например, губку, она через некоторое время восстановит свою форму?
Дело в том, что молекулы не только притягиваются друг к другу, но и отталкиваются. Если расстояние между ними станет очень малым (немного меньше размера молекулы), то межмолекулярное отталкивание становится более сильным, чем притяжение. Попробуйте сжать, например, монетку. Вы не сможете заметно уменьшить ее размеры, так как молекулы монетки будут отталкиваться друг от друга. Так же вы не сможете заметно уменьшить объем жидкости даже с помощью мощного пресса.
Именно межмолекулярное притяжение и отталкивание удерживает молекулы жидкостей и твердых веществ на более или менее определенных расстояниях, которые приблизительно равны размерам самих молекул. В случае уменьшения расстояния молекулы начинают отталкиваться друг от друга, а в случае увеличения — притягиваться, поэтому как для сближения, так и для отдаления молекул необходимо приложить усилие.
Молекулы взаимодействуют между собой: они одновременно притягиваются и отталкиваются. Межмолекулярное взаимодействие проявляется на расстояниях, которые можно сравнить с размерами самих молекул.
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.
Химическая связь
Статья находится на проверке у методистов Skysmart.
Если вы заметили ошибку, сообщите об этом в онлайн-чат (в правом нижнем углу экрана).
Химическая связь и строение вещества
Все системы стремятся к равновесию и к уменьшению свободной энергии — так гласит один из постулатов химической термодинамики. Атомы, взаимодействующие в молекуле вещества, тоже подчиняются этому закону. Они стремятся образовать устойчивую конфигурацию — 8-электронную или 2-электронную внешнюю оболочку. Этот процесс взаимодействия называется химической связью, благодаря ему получаются молекулы и молекулярные соединения.
| Химическая связь — это взаимодействие между атомами в молекуле вещества, в ходе которого два электрона (по одному от каждого атома) образуют общую электронную пару либо электрон переходит от одного атома к другому. |
Как понятно из определения химической связи, при взаимодействии двух атомов один из них может притянуть к себе внешние электроны другого. Эта способность называется электроотрицательностью (ЭО). Атом с более высокой электроотрицательностью (ЭО) при образовании химической связи с другим атомом может вызвать смещение к себе общей электронной пары.
Механизм образования химической связи
Существует два механизма взаимодействия атомов:
обменный — предполагает выделение по одному внешнему электрону от каждого атома и соединение их в общую пару;
донорно-акцепторный — происходит, когда один атом (донор) выделяет два электрона, а второй атом (акцептор) принимает их на свою свободную орбиталь.
Независимо от механизма химическая связь между атомами сопровождается выделением энергии. Чем выше ЭО атомов, т. е. их способность притягивать электроны, тем сильнее и этот энергетический всплеск.
| Энергией связи называют ту энергию, которая выделяется при взаимодействии атомов. Она определяет прочность химической связи и по величине равна усилию, необходимому для ее разрыва. |
Также на прочность влияют следующие показатели:
Длина связи — расстояние между ядрами атомов. С уменьшением этого расстояния растет энергия связи и увеличивается ее прочность.
Кратность связи — количество электронных пар, появившихся при взаимодействии атомов. Чем больше это число, тем выше энергия и, соответственно, прочность связи.
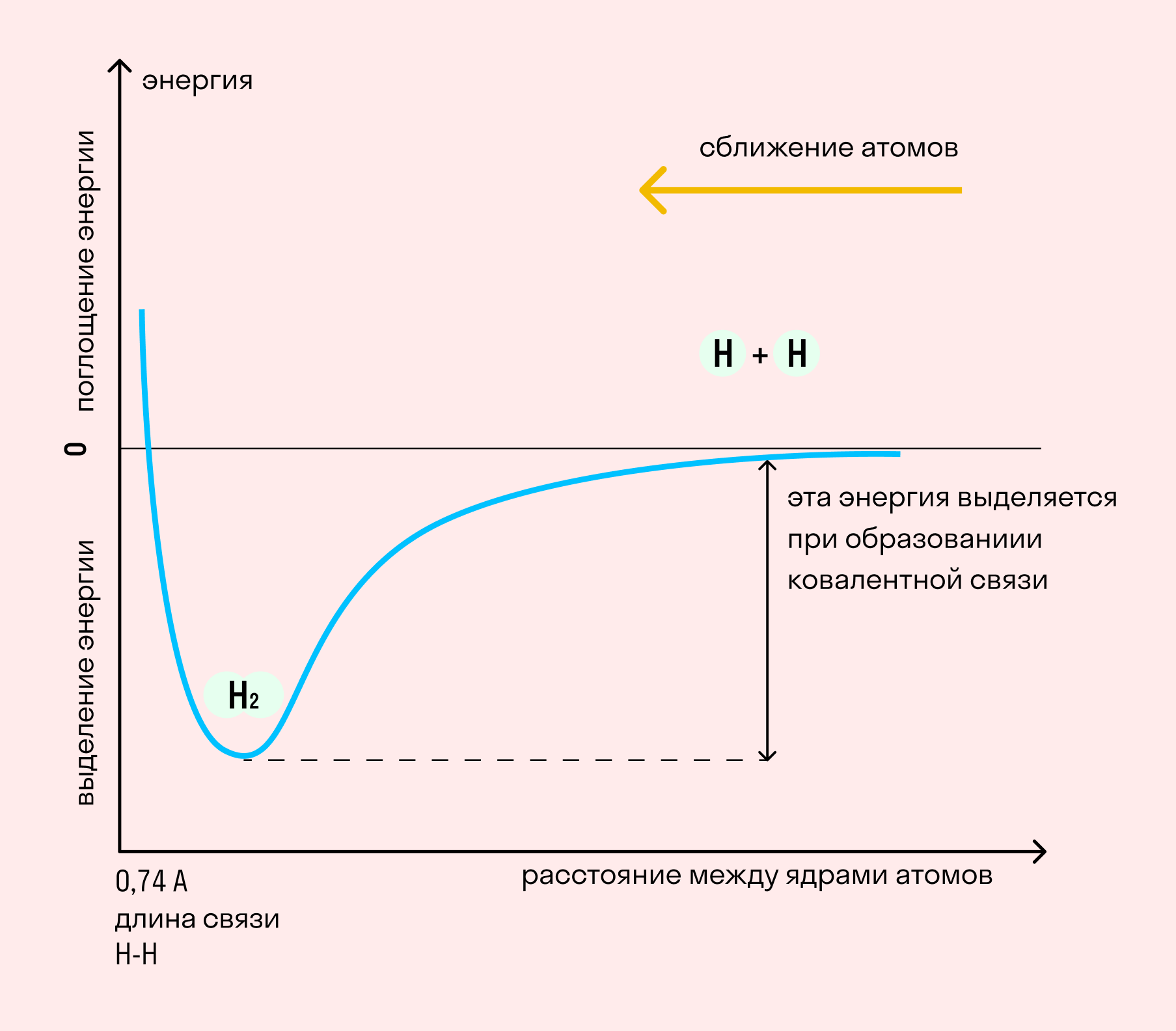
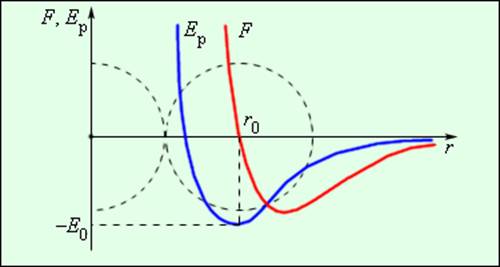
На примере химической связи в молекуле водорода посмотрим, как меняется энергия системы при сокращении расстояния между ядрами атомов. По мере сближения ядер электронные орбитали этих атомов начинают перекрывать друг друга, в итоге появляется общая молекулярная орбиталь. Неспаренные электроны через области перекрывания смещаются от одного атома в сторону другого, возникают общие электронные пары. Все это сопровождается нарастающим выделением энергии. Сближение происходит до тех пор, пока силу притяжения не компенсирует сила отталкивания одноименных зарядов.
Основные типы химических связей
Различают четыре вида связей в химии: ковалентную, ионную, металлическую и водородную. Но в чистом виде они встречаются редко, обычно имеет место наложение нескольких типов химических связей. Например, в молекуле фосфата аммония (NH4)3PO4присутствует одновременно ионная связь между ионами и ковалентная связь внутри ионов.
Также отметим, что при образовании кристалла от типа связи между частицами зависит, какой будет кристаллическая решетка. Если это ковалентная связь — образуется атомная решетка, если водородная — молекулярная решетка, а если ионная или металлическая — соответственно, будет ионная или металлическая решетка. Таком образом, влияя на тип кристаллической решетки, химическая связь определяет и физические свойства вещества: твердость, летучесть, температуру плавления и т. д.
Основные характеристики химической связи:
насыщенность — ограничение по количеству образуемых связей из-за конечного числа неспаренных электронов;
полярность — неравномерная электронная плотность между атомами и смещение общей пары электронов к одному из них;
направленность — ориентация связи в пространстве, расположение орбиталей атомов под определенным углом друг к другу.
Ковалентная связь
Как уже говорилось выше, этот тип связи имеет два механизма образования: обменный и донорно-акцепторный. При обменном механизме объединяются в пару свободные электроны двух атомов, а при донорно-акцепторном — пара электронов одного из атомов смещается к другому на его свободную орбиталь.
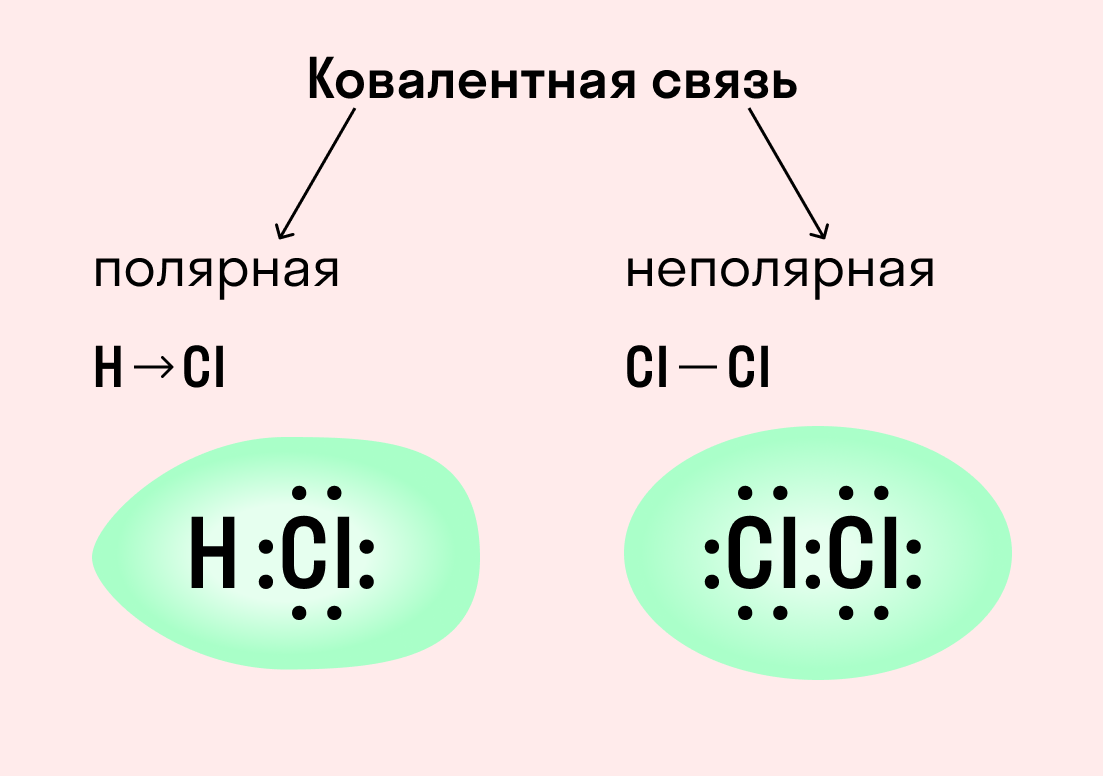
| Ковалентная связь — это процесс взаимодействия между атомами с одинаковыми или близкими радиусами, при котором возникает общая электронная пара. Если эта пара принадлежит в равной мере обоим взаимодействующим атомам — это неполярная связь, а если она смещается к одному из них — это полярная связь. |
Как вы помните, сила притяжения электронов определяется электроотрицательностью атома. Если у двух атомов она одинакова, между ними будет неполярная связь, а если один из атомов имеет большую ЭО — к нему сместится общая электронная пара и получится полярная химическая связь.
Ковалентная неполярная связь образуется в молекулах простых веществ, неметаллов с одинаковой ЭО: Cl2, O2, N2, F2 и других.
Посмотрим на схему образования этой химической связи. У атомов водорода есть по одному внешнему электрону, которые и образуют общую пару.
Ковалентная полярная связь характерна для неметаллов с разным уровнем ЭО: HCl, NH3,HBr, H2O, H2S и других.
Посмотрим схему такой связи в молекуле хлороводорода. У водорода имеется один свободный электрон, а у хлора — семь. Таким образом, всего есть два неспаренных электрона, которые соединяются в общую пару. Поскольку в данном случае ЭО выше у хлора, эта пара смещается к нему.
Другой пример — молекула сероводорода H2S. В данном случае мы видим, что каждый атом водорода имеет по одной химической связи, в то время как атом серы — две. Количество связей определяет валентность атома в конкретном соединении, поэтому валентность серы в сероводороде — II.
Число связей, которые могут быть у атома в молекуле вещества, называется валентностью.
Характеристики ковалентной связи:
Ионная связь
Как понятно из названия, данный тип связи основан на взаимном притяжении ионов с противоположными зарядами. Он возможен между веществами с большой разницей ЭО — металлом и неметаллом. Механизм таков: один из атомов отдает свои электроны другому атому и заряжается положительно. Второй атом принимает электроны на свободную орбиталь и получает отрицательный заряд. В результате этого процесса образуются ионы.
| Ионная связь — это такое взаимодействие между атомами в молекуле вещества, итогом которого становится образование и взаимное притяжение ионов. |
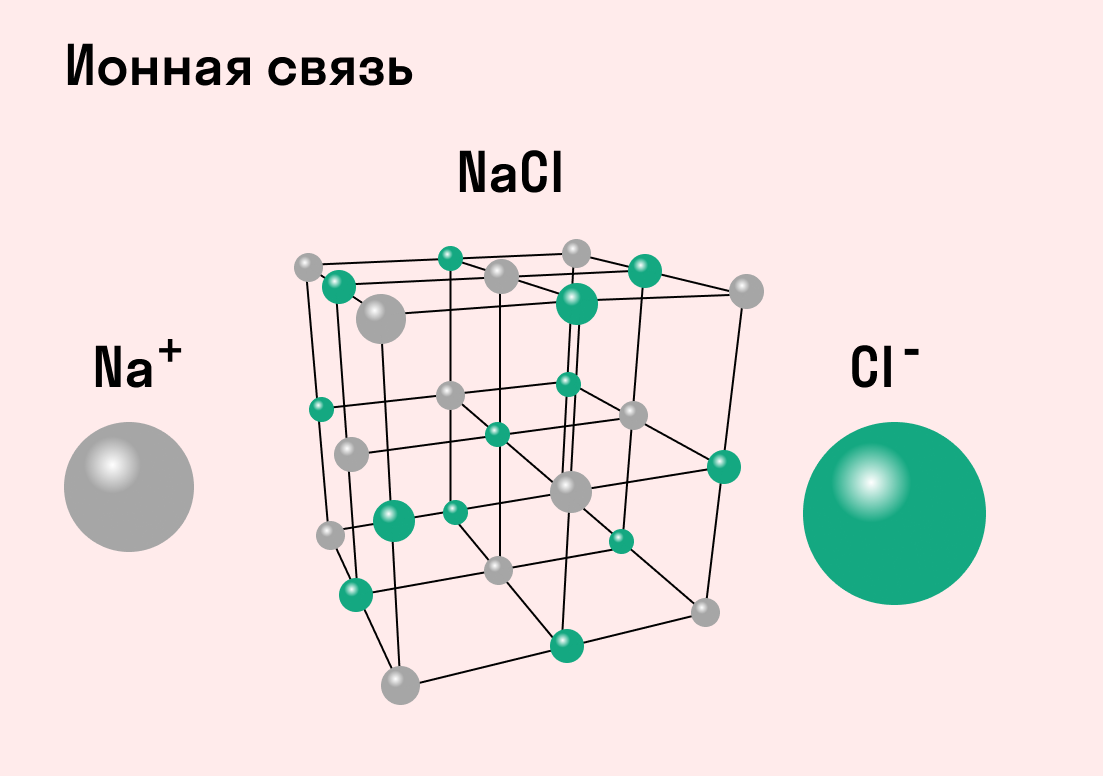
Разноименно заряженные ионы стремятся друг к другу за счет кулоновского притяжения, которое одинаково направлено во все стороны. Благодаря этому притяжению образуются ионные кристаллы, в решетке которых заряды ионов чередуются. У каждого иона есть определенное количество ближайших соседей — оно называется координационным числом.
Обычно ионная связь появляется между атомами металла и неметалла в таких соединениях, как NaF, CaCl2, BaO, NaCl, MgF2, RbI и других. Ниже схема ионной связи в молекуле хлорида натрия.
Характеристики ионной связи:
не имеет направленности.
Ковалентная и ионная связь в целом похожи, и одну из них можно рассматривать, как крайнее выражение другой. Но все же между ними есть существенная разница. Сравним эти виды химических связей в таблице.
Характеризуется появлением электронных пар, принадлежащих обоим атомам.
Характеризуется появлением и взаимным притяжением ионов.
Общая пара электронов испытывает притяжение со стороны обоих ядер атомов.
Ионы с противоположными зарядами подвержены кулоновскому притяжению.
Имеет направленность и насыщенность.
Ненасыщенна и не имеет направленности.
Количество связей, образуемых атомом, называется валентностью.
Количество ближайших соседей атома называется координационным числом.
Образуется между неметаллами с одинаковой или не сильно отличающейся ЭО.
Образуется между металлами и неметаллами — веществами со значимо разной ЭО.
Металлическая связь
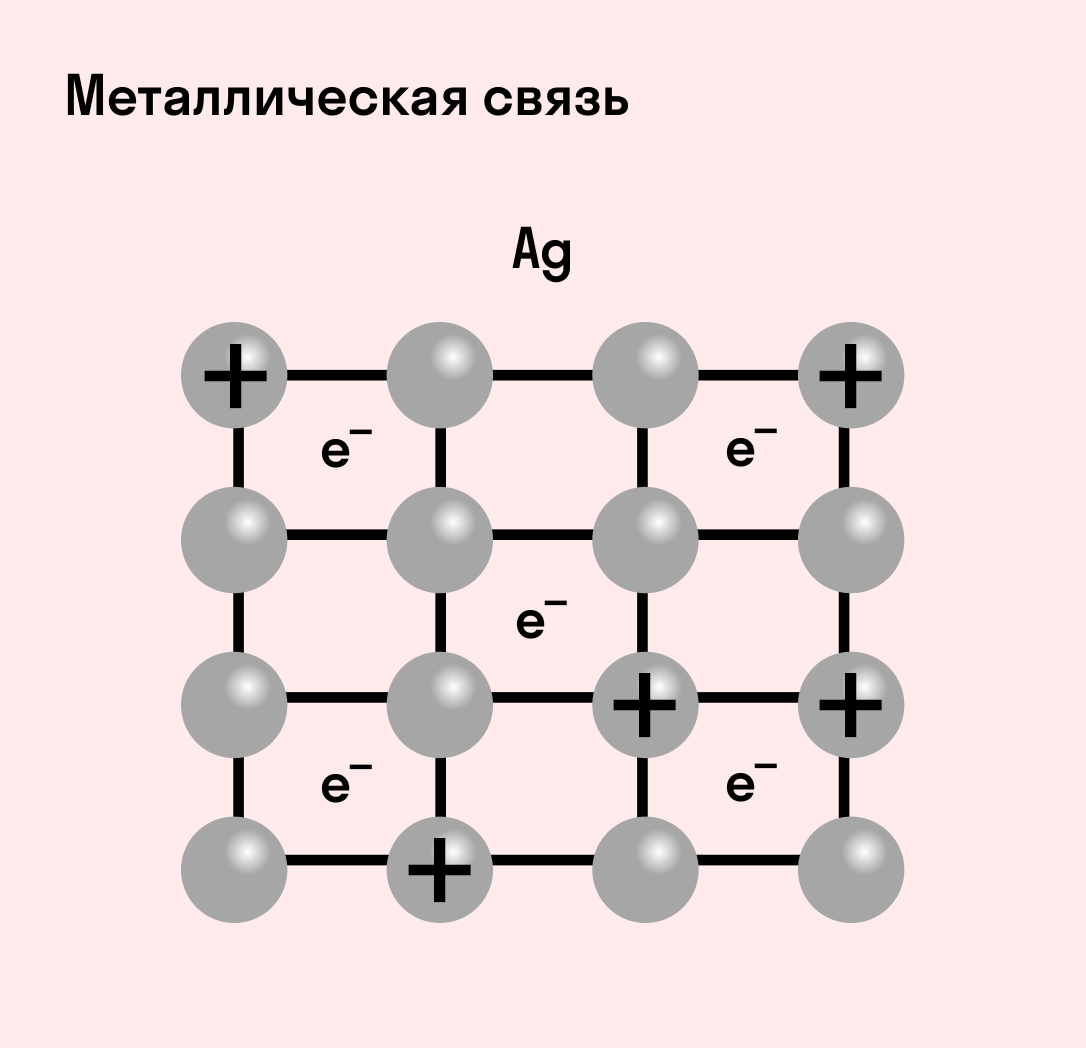
Отличительная особенность металлов в том, что их атомы имеют достаточно большие радиусы и легко отдают свои внешние электроны, превращаясь в положительно заряженные ионы (катионы). В итоге получается кристаллическая решетка, в узлах которой находятся ионы, а вокруг беспорядочно перемещаются электроны проводимости, образуя «электронное облако» или «электронный газ».
Свободные электроны мигрируют от одного иона к другому, временно соединяясь с ними и снова отрываясь в свободное плавание. Этот механизм по своей природе имеет сходство с ковалентной связью, но взаимодействие происходит не между отдельными атомами, а в веществе.
| Металлическая связь — это взаимодействие положительных ионов металлов и отрицательно заряженных электронов, которые являются частью «электронного облака», рассеянного по всему объему вещества. |
Наличие такого «электронного облака», которое может прийти в направленное движение, обусловливает электропроводность металлов. Другие их качества — пластичность и ковкость, объясняются тем, что ионы в кристаллической решетке легко смещаются. Поэтому металл при ударном воздействии способен растягиваться, но не разрушаться.
Характеристики металлической связи:
Металлическая связь присуща как простым веществам — таким как Na, Ba, Ag, Cu, так и сложным сплавам — например, AlCr2, CuAl11Fe4, Ca2Cu и другим.
Схема металлической связи:
M — металл,
n — число свободных внешних электронов.
К примеру, у железа в чистом виде на внешнем уровне есть два электрона, поэтому его схема металлической связи выглядит так:
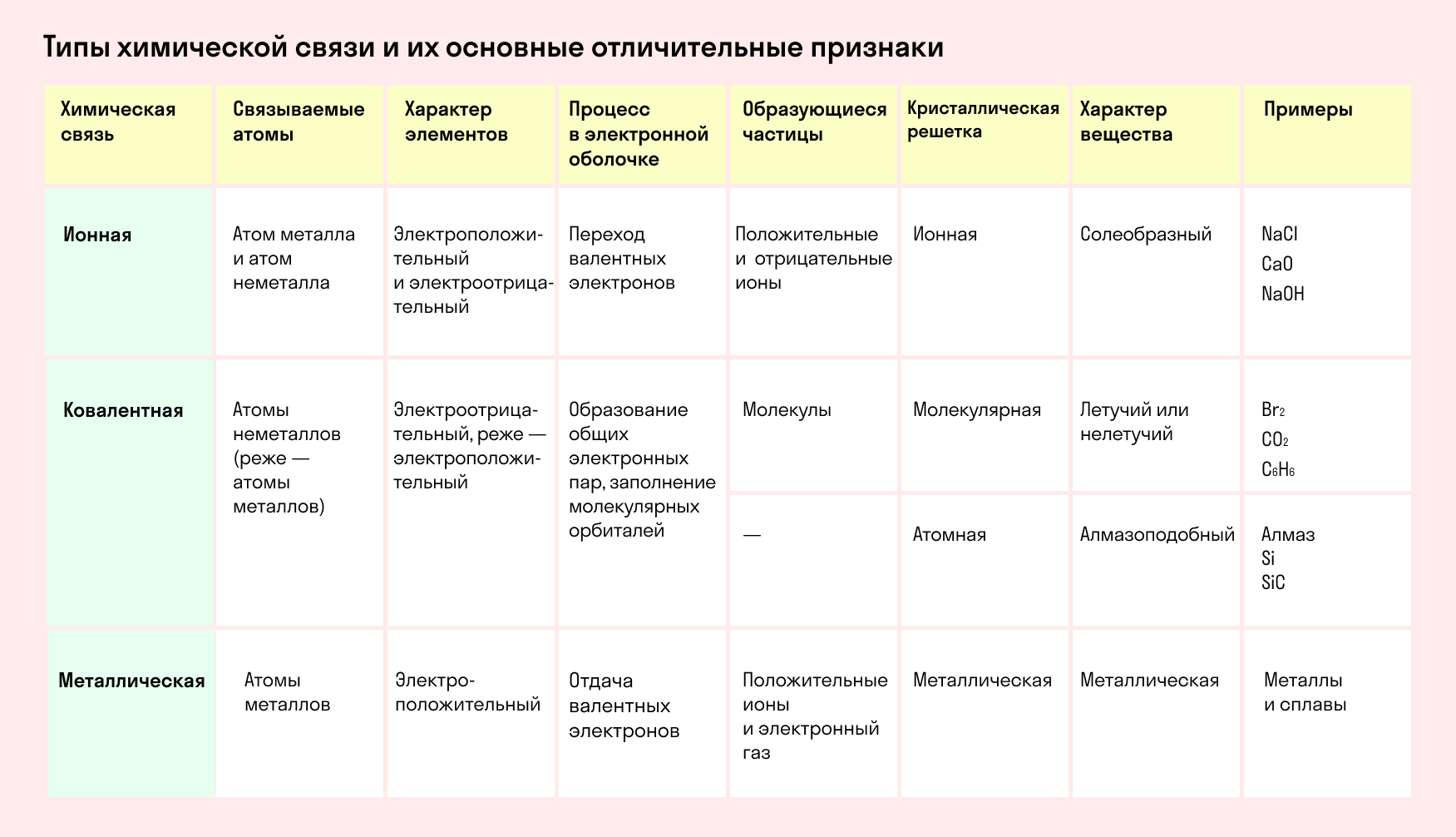
Обобщим все полученные знания. Таблица ниже описывает кратко химические связи и строение вещества.
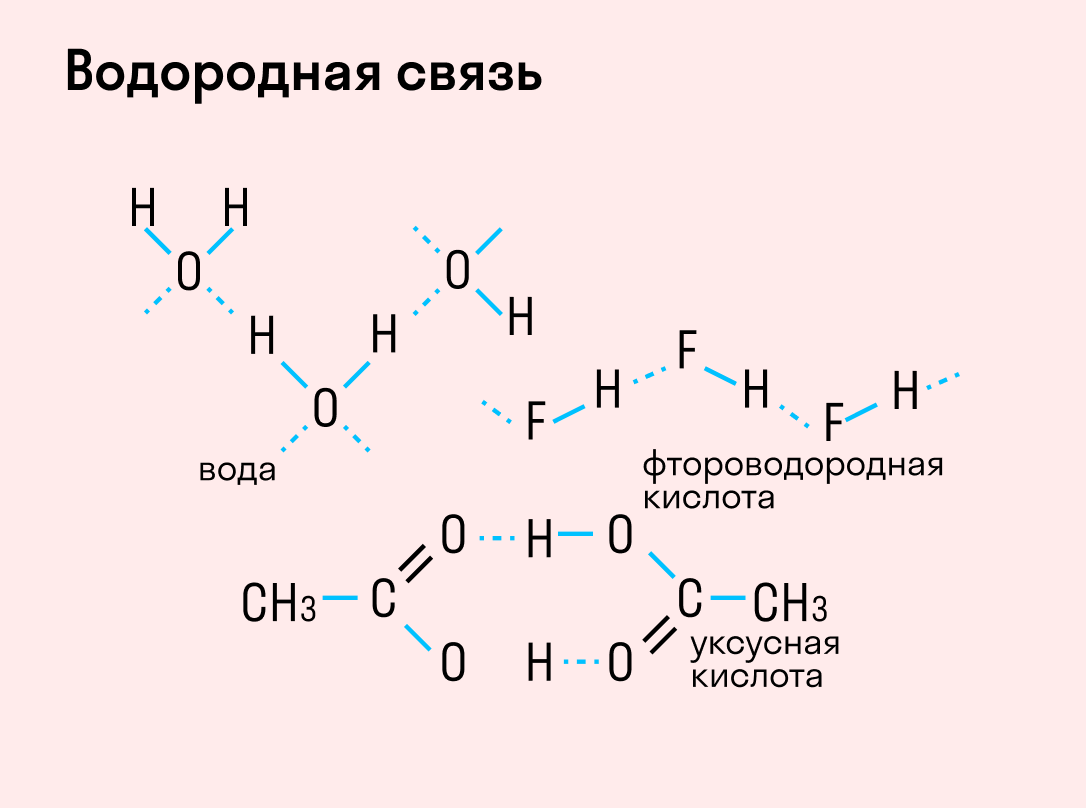
Водородная связь
Данный тип связи в химии стоит отдельно, поскольку он может быть как внутри молекулы, так и между молекулами. Как правило, у неорганических веществ эта связь происходит между молекулами.
| Водородная связь образуется между молекулами, содержащими водород. Точнее, между атомами водорода в этих молекулах и атомами с большей ЭО в других молекулах вещества. |
Объясним подробнее механизм этого вида химической связи. Есть молекулы А и В, содержащие водород. При этом в молекуле А есть электроотрицательные атомы, а в молекуле В водород имеет ковалентную полярную связь с другими электроотрицательными атомами. В этом случае между атомом водорода в молекуле В и электроотрицательным атомом в молекуле А образуется водородная связь.
Такое взаимодействие носит донорно-акцепторный характер. Донором электронов в данном случае выступают электроотрицательные элементы, а акцептором — водород.
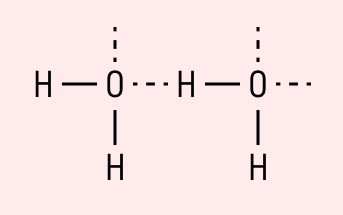
Графически водородная связь обозначается тремя точками. Ниже приведена схема такого взаимодействия на примере молекул воды.
Характеристики водородной связи:
Кратко о химических связях
Итак, самое главное. Химической связью называют взаимодействие атомов, причиной которого является стремление системы приобрести устойчивое состояние. Во время взаимодействия свободные внешние электроны атомов объединяются в пары либо внешний электрон одного атома переходит к другому.
Образование химической связи сопровождается выделением энергии. Эта энергия растет с увеличением количества образованных электронных пар и с сокращением расстояния между ядрами атомов.
Основные виды химических связей: ковалентная (полярная и неполярная), ионная, металлическая и водородная. В отличие от всех остальных водородная ближе к молекулярным связям, поскольку может быть как внутри молекулы, так и между разными молекулами.
Как определить тип химической связи:
Ковалентная полярная связь образуется в молекулах неметаллов между атомами со сходной ЭО.
Ковалентная неполярная связь имеет место между атомами с разной ЭО.
Ионная связь ведет к образованию и взаимному притяжению ионов. Она происходит между атомами металла и неметалла.
Металлическая связь бывает только между атомами металлов. Это взаимодействие положительных ионов в кристаллической решетке и свободных отрицательных электронов. Масса рассеянных по всему объему свободных электронов представляет собой «электронное облако».
Водородная связь появляется при условии, что есть атом с высокой ЭО и атом водорода, связанный с другой электроотрицательной частицей ковалентной связью.
Химическая связь и строение молекулы: типом химической связи определяется кристаллическая решетка вещества: ионная, металлическая, атомная или молекулярная.
Определить тип химической связи в 8 классе поможет таблица.
Основные положения МКТ
Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химических веществ.
В основе молекулярно-кинетической теории лежат три основных положения:
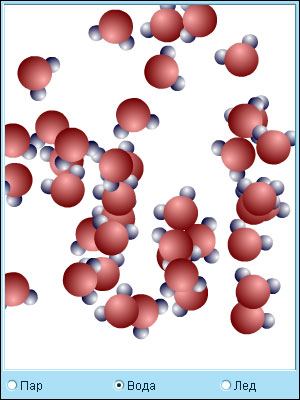
1. Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов («элементарных молекул»). Молекулы химического вещества могут быть простыми и сложными, т.е. состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы.
2. Атомы и молекулы находятся в непрерывном хаотическом движении.
3. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
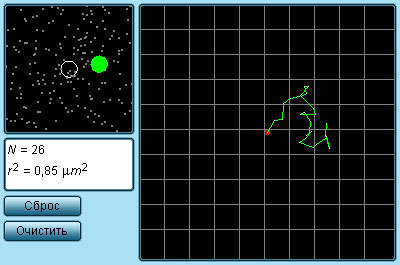
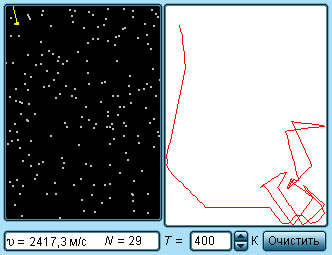
Траектория броуновской частицы
Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение. Это тепловое движение мельчайших микроскопических частиц, взвешенных в жидкости или газе. Оно было открыто английским ботаником Робертом Броуном в 1827 г. Броуновские частицы движутся под влиянием беспорядочных ударов молекул. Из-за хаотического теплового движения молекул эти удары никогда не уравновешивают друг друга. В результате скорость броуновской частицы беспорядочно меняется по модулю и направлению, а ее траектория представляет собой сложную зигзагообразную кривую (рис. 3.1.1). Теория броуновского движения была создана А.Эйнштейном в 1905 г. Экспериментально теория Эйнштейна была подтверждена в опытах французского физика Жана Перрена, проведенных в 1908–1911 гг.