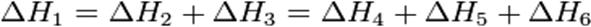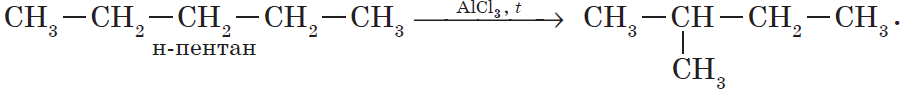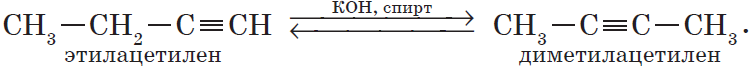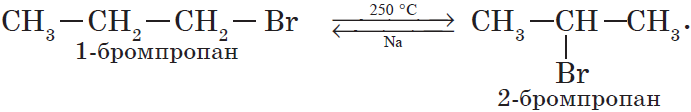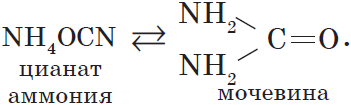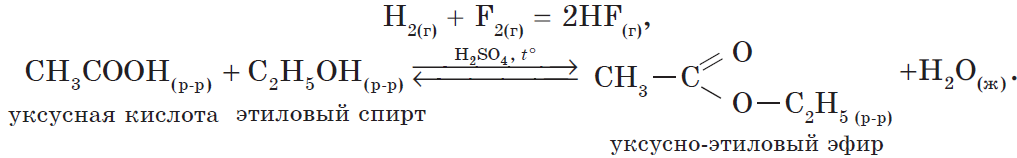Что такое экзотермическая реакция и эндотермическая реакция
Тепловой эффект реакции: экзо- и эндотермические реакции; закон Гесса; (стандартная) теплота образования вещества.



Закон Гесса — Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Иными словами, количество теплоты, выделяющееся или поглощающееся при каком-либо процессе, всегда одно и то же, независимо от того, протекает ли данноехимическое превращение в одну или в несколько стадий (при условии, что температура, давление и агрегатные состояния веществ одинаковы). Например, окислениеглюкозы в организме осуществляется по очень сложному многостадийному механизму, однако суммарный тепловой эффект всех стадий данного процесса равен теплоте сгорания глюкозы.
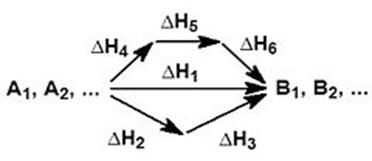
На рисунке приведено схематическое изображение некоторого обобщенного химического процесса превращения исходных веществ А1, А2… в продукты реакции В1, В2…, который может быть осуществлен различными путями в одну, две или три стадии, каждая из которых сопровождается тепловым эффектом ΔHi. Согласно закону Гесса, тепловые эффекты всех этих реакций связаны следующим соотношением:
Закон открыт русским химиком Г. И. Гессом в 1840 г.; он является частным случаем первого начала термодинамикиприменительно к химическим реакциям. Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать тепловые эффекты самых разнообразных химических процессов; для этого обычно используют ряд следствий из него.
Скорость реакции и факторы, влияющие на нее. Гомогенные и гетерогенные реакции. Закон действующих масс. Константа скорости реакции. Порядок и молекулярность реакции. Правило Вант-Гоффа
Скорость химической реакции — изменение количества одного из реагирующих веществ за единицу времени в единице реакционного пространства. Скорость химической реакции — величина всегда положительная, поэтому, если она определяется по исходному веществу (концентрация которого убывает в процессе реакции), то полученное значение умножается на −1.
Мономолекулярные реакции — реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д.) Бимолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных)Тримолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении трех частиц. Реакции с молекулярностью более трёх неизвестны.
Порядок реакции по данному веществу — показатель степени при концентрации этого вещества в кинетическом уравнении реакции.Правило Вант-Гоффа — эмпирическое правило, позволяющее в первом приближении оценить влияние температуры на скорость химической реакции в небольшом температурном интервале (обычно от 0 °C до 100 °C). При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два—четыре раза.
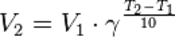
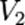
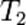
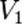
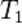
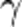
Разница между эндотермическими и экзотермическими реакциями
Химические реакции можно разделить на две группы как эндотермические реакции и экзотермические реакции в соответствии с переносом энергии между окружающей средой и системой, в которой происходит реак
Содержание:
Химические реакции можно разделить на две группы как эндотермические реакции и экзотермические реакции в соответствии с переносом энергии между окружающей средой и системой, в которой происходит реакция. Чтобы классифицировать конкретную химическую реакцию как эндотермическую или экзотермическую, мы можем рассчитать изменение энтальпии между реагентами и продуктами. Если нет, мы можем наблюдать изменение температуры реакционной смеси. Основное различие между эндотермическими и экзотермическими реакциями заключается в том, что эндотермические реакции поглощают энергию от окружающих, тогда как экзотермические реакции выделяют энергию для окружающих.
Ключевые области покрыты
1. Что такое эндотермические реакции
— определение, свойства, примеры
2. Что такое экзотермические реакции
— определение, свойства, примеры
3. В чем разница между эндотермическими и экзотермическими реакциями
— Сравнение основных различий
Ключевые термины: Горение, Эндотермический, Энтальпия, Экзотермический, Тепловой, Внутренняя энергия
Что такое эндотермические реакции
& delta; H является изменение энтальпии, которое происходит после реакции,
HC а также HD являются энтальпиями продуктов C и D соответственно
HA а также HB энтальпии реагентов A и B соответственно.
Рисунок 1: Энтальпии реагентов и продуктов эндотермической реакции
Эндотермическую реакцию можно легко распознать, прикоснувшись к химическому стакану или пробирке, где происходит реакция. Стакан будет чувствовать себя холоднее, чем раньше. Это потому, что он поглощает энергию извне.
Примеры эндотермических реакций
Обратите внимание, что «тепло» входит в правую часть уравнения реакции. Это указывает на поглощение тепла системой.
Что такое экзотермические реакции
Изменение энтальпии в настоящее время является отрицательным значением, поскольку внутренняя энергия реагентов меньше из-за выделения энергии. Температура системы будет увеличиваться по мере протекания экзотермической реакции. Следовательно, можно догадаться, является ли конкретная химическая реакция эндотермической или экзотермической, просто прикоснувшись к стенке контейнера, где происходит реакция. При экзотермической реакции контейнер станет теплее.
Рисунок 2: Энтальпии реагентов и продуктов экзотермической реакции
Примеры экзотермических реакций
Разница между эндотермическими и экзотермическими реакциями
Определение
температура
Эндотермические реакции: Снижение температуры при прогрессировании эндотермических реакций.
Экзотермические реакции: Повышение температуры при прогрессировании экзотермических реакций.
энтальпия
Эндотермические реакции: Энтальпия реагентов ниже, чем у продуктов в эндотермических реакциях.
Экзотермические реакции: Энтальпия реагентов выше, чем у продуктов экзотермических реакций.
Изменение энтальпии
Эндотермические реакции: Изменение энтальпии (ΔH) является положительным значением для эндотермических реакций.
Экзотермические реакции: Изменение энтальпии (ΔH) является отрицательным значением для экзотермических реакций.
энергии
Эндотермические реакции: Энергия должна быть отдана системе в эндотермических реакциях.
Экзотермические реакции: Энергия высвобождается из системы в результате эндотермических реакций.
Заключение
Химические реакции подразделяются на эндотермические и экзотермические реакции в соответствии с переносом энергии между системой и окружающей средой. Основное различие между эндотермическими и экзотермическими реакциями заключается в том, что эндотермические реакции поглощают энергию из окружающей среды, тогда как экзотермические реакции выделяют энергию в окружающую среду.. Каждая химическая реакция может быть сгруппирована в эти две категории путем вычисления изменения энтальпии в реакции.
Рекомендации:
1. «Эндотермические реакции». Эндотермические реакции, примеры эндотермических реакций | [электронная почта защищена] Н.П., Н.Д. Web.
Классификация химических реакций в неорганической и органической химии
Теория к заданию 19 из ЕГЭ по химии
Классификация химических реакций в неорганической и органической химии
Химические реакции, или химические явления, — это процессы, в результате которых из одних веществ образуются другие, отличающиеся от них по составу и (или) строению.
При химических реакциях обязательно происходит изменение веществ, при котором рвутся старые и образуются новые связи между атомами.
Химические реакции следует отличать от ядерных реакций. В результате химической реакции общее число атомов каждого химического элемента и его изотопный состав не меняются. Иное дело ядерные реакции — процессы превращения атомных ядер в результате их взаимодействия с другими ядрами или элементарными частицами, например, превращение алюминия в магний:
Классификация химических реакций многопланова, т.е. в ее основу могут быть положены различные признаки. Но под любой из таких признаков могут быть отнесены реакции как между неорганическими, так и между органическими веществами.
Рассмотрим классификацию химических реакций по различным признакам.
Классификация химических реакций по числу и составу реагирующих веществ. Реакции, идущие без изменения состава вещества
В неорганической химии к таким реакциям можно отнести процессы получения аллотропных модификаций одного химического элемента, например:
В органической химии к этому типу реакций могут быть отнесены реакции изомеризации, которые идут без изменения не только качественного, но и количественного состава молекул веществ, например:
1. Изомеризация алканов.
Реакция изомеризации алканов имеет большое практическое значение, т.к. углеводороды изостроения обладают меньшей способностью к детонации.
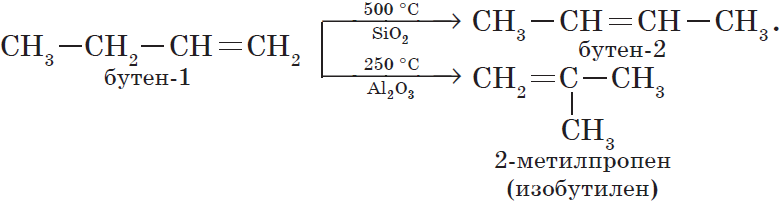
2. Изомеризация алкенов.
3. Изомеризация алкинов (реакция А. Е. Фаворского).
4. Изомеризация галогеналканов (А. Е. Фаворский).
5. Изомеризация цианата аммония при нагревании.
Впервые мочевина была синтезирована Ф. Велером в 1882 г. изомеризацией цианата аммония при нагревании.
Реакции, идущие с изменением состава вещества
Можно выделить четыре типа таких реакций: соединения, разложения, замещения и обмена.
1. Реакции соединения — это такие реакции, при которых из двух и более веществ образуется одно сложное вещество.
В неорганической химии все многообразие реакций соединения можно рассмотреть на примере реакций получения серной кислоты из серы:
1) получение оксида серы (IV):
$S+O_2=SO_2$ — из двух простых веществ образуется одно сложное;
2) получение оксида серы (VI):
3) получение серной кислоты:
$SO_3+H_2O=H_2SO_4$ — из двух сложных веществ образуется одно сложное.
Примером реакции соединения, при которой одно сложное вещество образуется из более чем двух исходных, может служить заключительная стадия получения азотной кислоты:
В органической химии реакции соединения принято называть реакциями присоединения. Все многообразие таких реакций можно рассмотреть на примере блока реакций, характеризующих свойства непредельных веществ, например этилена:
1) реакция гидрирования — присоединение водорода:
2) реакция гидратации — присоединение воды:
3) реакция полимеризации:
2. Реакции разложения — это такие реакции, при которых из одного сложного вещества образуется несколько новых веществ.
В неорганической химии все многообразие таких реакций можно рассмотреть на примере блока реакций получения кислорода лабораторными способами:
1) разложение оксида ртути (II):
$2HgO<→>↖
2) разложение нитрата калия:
$2KNO_3<→>↖
3) разложение перманганата калия:
$2KMnO_4<→>↖
В органической химии реакции разложения можно рассмотреть на примере блока реакций получения этилена в лаборатории и промышленности:
1) реакция дегидратации (отщепления воды) этанола:
2) реакция дегидрирования (отщепления водорода) этана:
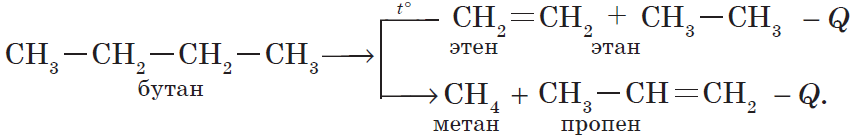
3) реакция крекинга (расщепления) пропана:
3. Реакции замещения — это такие реакции, в результате которых атомы простого вещества замещают атомы какого-либо элемента в сложном веществе.
В неорганической химии примером таких процессов может служить блок реакций, характеризующих свойства, например, металлов:
1) взаимодействие щелочных и щелочноземельных металлов с водой:
2) взаимодействие металлов с кислотами в растворе:
3) взаимодействие металлов с солями в растворе:
Предметом изучения органической химии являются не простые вещества, а только соединения. Поэтому как пример реакции замещения приведем наиболее характерное свойство предельных соединений, в частности метана, — способность его атомов водорода замещаться на атомы галогена:
Другой пример — бромирование ароматического соединения (бензола, толуола, анилина):
Обратим внимание на особенность реакций замещения у органических веществ: в результате таких реакций образуются не простое и сложное вещества, как в неорганической химии, а два сложных вещества.
В органической химии к реакциям замещения относят и некоторые реакции между двумя сложными веществами, например, нитрование бензола:
Она формально является реакцией обмена. То, что это реакция замещения, становится понятным только при рассмотрении ее механизма.
4. Реакции обмена — это такие реакции, при которых два сложных вещества обмениваются своими составными частями.
В неорганической химии это может быть блок реакций, характеризующих, например, свойства щелочей:
1) реакция нейтрализации, идущая с образованием соли и воды:
2) реакция между щелочью и солью, идущая с образованием газа:
3) реакция между щелочью и солью, идущая с образованием осадка:
В органической химии можно рассмотреть блок реакций, характеризующих, например, свойства уксусной кислоты:
2) реакция, идущая с образованием газа:
3) реакция, идущая с образованием осадка:
Классификация химических реакций по изменению степеней окисления химических элементов, образующих вещества
Реакции, идущие с изменением степеней окисления элементов, или окислительно-восстановительные реакции.
К ним относится множество реакций, в том числе все реакции замещения, а также те реакции соединения и разложения, в которых участвует хотя бы одно простое вещество, например:
Как вы помните, сложные окислительно-восстановительные реакции составляются с помощью метода электронного баланса:
В органической химии ярким примером окислительно-восстановительных реакций могут служить свойства альдегидов:
1. Альдегиды восстанавливаются в соответствующие спирты:
2. Альдегиды окисляются в соответствующие кислоты:
Реакции, идущие без изменения степеней окисления химических элементов.
К ним, например, относятся все реакции ионного обмена, а также:
Классификация химических реакций по тепловому эффекту
По тепловому эффекту реакции делят на экзотермические и эндотермические.
Эти реакции протекают с выделением энергии.
К ним относятся почти все реакции соединения. Редкое исключение составляют эндотермические реакции синтеза оксида азота (II) из азота и кислорода и реакция газообразного водорода с твердым иодом:
Экзотермические реакции, которые протекают с выделением света, относят к реакциям горения, например:
Гидрирование этилена — пример экзотермической реакции:
Она идет при комнатной температуре.
Эндотермические реакции
Эти реакции протекают с поглощением энергии.
Очевидно, что к ним относятся почти все реакции разложения, например:
а) обжиг известняка:
Количество выделенной или поглощенной в результате реакции энергии называют тепловым эффектом реакции, а уравнение химической реакции с указанием этого эффекта называют термохимическим уравнением, например:
Классификация химических реакций по агрегатному состоянию реагирующих веществ (фазовому составу)
Это реакции, в которых реагирующие вещества и продукты реакции находятся в разных агрегатных состояниях (в разных фазах):
Это реакции, в которых реагирующие вещества и продукты реакции находятся в одном агрегатном состоянии (в одной фазе):
Классификация химических реакций по участию катализатора
Некаталитические реакции идут без участия катализатора:
Каталитические реакции идут с участием катализатора:
Так как все биологические реакции, протекающие в клетках живых организмов, идут с участием особых биологических катализаторов белковой природы — ферментов, все они относятся к каталитическим или, точнее, ферментативным.
Классификация химических реакций по направлению
Необратимые реакции протекают в данных условиях только в од ном направлении.
К ним можно отнести все реакции обмена, сопровождающиеся образованием осадка, газа или малодиссоциирующего вещества (воды), и все реакции горения.
Обратимые реакции в данных условиях протекают одновременно в двух противоположных направлениях.
Таких реакций подавляющее большинство.
В органической химии признак обратимости отражают названия-антонимы процессов:
Обратимы все реакции этерификации (противоположный процесс, как вы знаете, носит название гидролиза) и гидролиза белков, сложных эфиров, углеводов, полинуклеотидов. Обратимость лежит в основе важнейшего процесса в живом организме — обмена веществ.
Реакции экзотермические и эндотермические
Известно, что одни химические реакции для своего течения требуют нагрева, а другие происходят даже при глубоком охлаждении. Иногда химические превращения вызываются облучением реагентов светом, а иногда сопровождаются выделением большого количества света и тепла. Вам известны реакции горения, которые сопровождаются выделением теплоты и света, например, горения угля. Существует немало других реакций, при которых выделяется теплота. Так, при взаимодействии кальций оксида с водой (гашения извести) выделяется значительное количество теплоты:
CaO + H2O = Ca (OH) 2 + Q;
В экзо- термических реакциях теплота выделяется. В эндотермических реакциях теплота поглощается.
Теплота выделяется также при реакций между кислотой и щелочью.
Химические реакции, протекающие с выделением тепла, называют экзотермическими (от греческого «экзо» – «наружу»).
Существуют реакции, при которых теплота поглощается. Для возникновения и развития таких реакций требуется нагрев. Например, известняк превращается в жженое известь в процессе непрерывного нагрева, расписание калий перманганата, в результате которого добывают кислород, тоже происходит при нагревании:
2KMnO4 = K2MnO4 + MnO2 + O2 – Q.
Химические реакции, протекающие с поглощением теплоты, называют эндотермическими (от греческого «эндо» – «внутрь»).
Чтобы показать выделение или поглощение теплоты, в химическом уравнении после формул продуктов реакции дописывают Q:
«+ Q» (если теплота выделяется);
«- Q» (если теплота поглощается).
Реакции, при которых теплота выделяется, называют экзотермическими, а реакции, при которых теплота поглощается, называют эндотермическими.
Отрасль химии, которая исследует тепловые эффекты при химических реакций, называется термохимией.
Количество теплоты, которая поглощается или выделяется при химических реакций, называют тепловым эффектом реакции (обозначается: ΔH («дельта-аш»)).
Все реакции проходят с определенным тепловым эффектом: или с выделением теплоты, или с ее поглощением. Если количество теплоты незначительна, то заметить тепловой эффект реакции довольно трудно.
«Тепловой эффект реакции. Экзотермические и эндотермические реакции. Термохимические уравнения.»
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «УЧЕБНО-ВОСПИТАТЕЛЬНЫЙ КОМПЛЕКС «ГАРМОНИЯ» ГОРОДА ДОНЕЦКА»
МЕТОДИЧЕСКАЯ РАЗРАБОТКА ОТКРЫТОГО УРОКА
ПО ХИМИИ ДЛЯ 11 КЛАССА НА ТЕМУ:
«Тепловой эффект реакции. Экзотермические и эндотермические реакции. Термохимические уравнения.»
Дикань Ирина Владимировна
Учитель химии «Муниципального общеобразовательного учреждения
«Учебно-воспитательного комплекса «Гармония» г.Донецка»
ТЕМА УРОКА: ТЕПЛОВОЙ ЭФФЕКТ РЕАКЦИИ. ЭКЗОТЕРМИЧЕСКИЕ И ЭНДОТЕРМИЧЕСКИЕ РЕАКЦИИ. ТЕРМОХИМИЧЕСКИЕ УРАВНЕНИЯ.
Обучающая цель – расширить представление о химических реакциях на примере эндотермических и экзотермических реакций. Ознакомить учеников с понятием «тепловой эффект химической реакции», термохимические уравнения.
Развивающая цель – развивать у учащихся умение наблюдать, анализировать природные явления и проводимый химический эксперимент; совершенствовать навыки ведения наблюдений, устанавливать причинно-следственные связи, делать выводы и заключения. развивать навыки и умения составлять термохимические уравнения реакций
Воспитательная цель – воспитывать у учащихся коммуникативных навыков,чувства товарищества и взаимопомощи, умение работать в парах. Выполняя лабораторные опыты соблюдать технику безопасности ; воспитывать бережливое отношение к окружающей среде, культуру общения и умения сотрудничать в коллективе.
Тип урока : комбинированный урок усвоения знаний, умений и навыков,и творческого приложения, их на практике.
Оборудование: Периодическая система химических элементов Д. И. Менделеева, таблица растворимости, ряд активности металлов, плакат с правилами техники безопасности в кабинете химии.
Демонстрация: Реакции екзотермические, ендотэрмические.
Проверка домашнего задания
Актуализация опорных знаний
Что такое степень окисления? Какие правила необходимо вспомнить, чтобы определить степень окисления атомов в веществе? Расставьте степень окисления в веществах. HN 3 ; NO ; N 2 O 3 ; NO 2 ; NHO 3 ; HNO 2 ; H 2 SO 4 ; K 2 MnO 4
Расставьте степень окисления атомов в веществах. Какие атомы являются окислителями, а какие восстановителями?
б) N 0 – 3 N +3 /восстановление /
Где идет процесс окисление,а где восстановление?
1.Расставьте коэффициенты в уравнениях реакций методом электронного баланса. Укажите окислители и восстановители.
2. Запишите уравнение реакций, укажите среди них уравнение ОВР. Последнее запишите в ионной форме.
3.Осуществите превращение. Укажите среди уравнения ОВР. Последнее уравнение запишите в ионной форме.
IV . Изучение нового материала.
Тепловой эффект химических реакций. Термохимические уравнения.
2 Mg + O 2 = 2 MgO + Q ;
2 HI + Cl 2 = I 2 +2 HCl + Q
N 2 + O 2 = 2 NO – 180 кДЖ
*Тепловой эффект показывает разницу между внутренней энергии исходных веществ и продуктов реакции:
*Термохимическое уравнение – уравнение в котором определенно тепловой эффект химической реакции:
V . Обобщение и систематизация полученных знаний.
Задача 1. Вычислите, какое количество тепла выделится при сжигании 3м 3 метана, если термохимическое уравнение горения метана:
V CH 4 =3м 3 134 моль – x кДж
Ответ: Q = 119394 кДж
Задача 2. Вычислите количество теплоты, которое нужно потратить на розложение NH 3 количеством вещества 6 моль, если тепловой эффект реакции составляет 92 кДж.
Задача 3. Какое количество теплоты выделится при сгорании 500 г угля, если тепловой эффект реакции 394 кДж?
Вариант № 1 Вычислите количество теплоты, которое выделится при горении серы массой 32 г, если тепловой эффект реакции 310 кДж.
Вариант № 3 Вычислите количество теплоты, которое выделится при горении водорода массой 100 г, если тепловой эффект реакции 484 кДж.
Вариант № 4 При сжигании 26 г ацетилена выделилось 1299,2 кДж теплоты. Найдите тепловой эффект реакции:
Задача № 5. Какой объем кислорода (при н.у.) выделится в результате реакции, термохимическое уравнение которой
2KClO3 = 2KCl + 3O2 – 91 кДж,
если на разложение бертолетовой соли было затрачено 182 кДж теплоты.
При выполнении работы осуществляется индивидуальная помощь учителя.
Первые 3 работы оцениваются.Устная проверка ( 2 ученика комментируют решение )
Что сегодня вам показалось самым интересным?
Что понравилось в нашей работе и что не понравилось?
По учебнику § 12 № 4,9,10.
1. Рудзитис Г.Е., Фельдман Ф.Г. Химия. 11 класс: учеб. для общеобразовательных организаций: базовый уровень. – М.: Просвещение, 2016. – 224 с.
2. Денисова В. Г. Химия 11 класс: Поурочные планы [Текст]: учеб. пособие для преподавателей / В. Г Денисова :- Волгоград.: «Учитель», 2003. – 208 с.
4. Материалы сети интернет.
Представьте себя химиком- технологом на заводе и охарактеризуйте химическую реакцию по всем известным вам признакам. Предложите условия, при которых скорость реакции будет максимальной.
Представьте себя химиком- технологом на заводе и охарактеризуйте химическую реакцию по всем известным вам признакам. Предложите условия, при которых скорость реакции будет максимальной.
Представьте себя химиком- технологом на заводе и охарактеризуйте химическую реакцию по всем известным вам признакам. Предложите условия,при которых скорость реакции будет максимальной.
Представьте себя химиком- технологом на заводе и охарактеризуйте химическую реакцию по всем известным вам признакам. Предложите условия,при которых скорость реакции будет максимальной.
Представьте себя химиком- технологом на заводе и охарактеризуйте химическую реакцию по всем известным вам признакам. Предложите условия,при которых скорость реакции будет максимальной.
2 Z n + O 2 = 2 Z n O + Q кДж ΔH