Что такое эмболизация вен пищевода
Портальная гипертензия
Чаще всего портальная гипертензия развивается у больных с циррозом печени и является одним из факторов, приводящим к летальному исходу при данном заболевании. Для портальной гипертензии характерно расширение вен передней брюшной стенки, геморроидальных вен и вен пищевода. Печеночная недостаточность при циррозе печени приводит к недостаточной выработке белков свертывания крови, поэтому у этих пациентов повышенная кровоточивость. Этим обусловлена высокая летальность от кровотечений при портальной гипертензии. Даже при современном состоянии медицины летальность при кровотечении из варикозно расширенных вен составляет более 50%.
Лечение портальной гипертензии в Инновационном сосудистом центре
В Инновационном сосудистом центре для лечения портальной гипертензии применяются как классические операции по созданию сплено-ренальных анастомозов, так и экстренные эндоваскулярные операции трансъягулярного портокавального шунтирования (TIPS).
Эндоваскулярные операции выполняются на ангиографическом комплексе с дополнительным использованием визуализации воротной вены с помощью УЗИ навигации. Такие вмешательства проводятся под местной анестезией с внутривенной седацией.
Операции сплено-ренального анастомоза выполняются у сохранных пациентов, перенесших кровотечение из варикозно-расширенных вен пищевода. Такие вмешательства мы выполняем под наркозом через доступ в левой боковой стенке живота с переходом на грудную клетку. Подобные вмешательства позволяют избежать смертельно-опасных осложнений портальной гипертензии.
 Причины и факторы риска
Причины и факторы риска
Портальная гипертензия возникает, когда что-то препятствует кровотоку через печень, повышая давление внутри воротной вены. Эта обструкция (закупорка) может быть внутрипеченочной, подпеченочной (внепеченочной) или надпеченочной.
Внутрипеченочные причины портальной гипертензии
Основной причиной возникновения гипертензии является цирроз (в 70% случаев). Есть много причин возникновения цирроза, наиболее распространенной из них является злоупотребление алкоголем. Цирроз печени может вызвать обширный фиброз (рубцевание). Интенсивное рубцевание препятствует прохождению жидкостей через печень. Фиброз окружает сосуды в печени, что затрудняет кровообращение.
В качестве причины портальной гипертензии выступает большое количество болезней:
Подпеченочные причины портальной гипертензии
Надпеченочные причины портальной гипертензии
Эти причины вызваны обструкцией кровотока из печени в сердце и могут включать:
Международные данные по распространенности портальной гипертензии неизвестны, хотя известно что 80% пациентов страдают от портальной гипертензии из-за внутрипеченочных причин, то есть цирроза печени.
Течение заболевания
Течение заболевания можно разбить на 4 стадии:
I стадия — начальная
Заболевание уже появилось, но ещё не может диагностироваться. Протекает бессимптомно, либо пациенты ощущают тяжесть в правом подреберье и легкое недомогание.
II стадия — умеренная
Появляются выраженные клинические симптомы заболевания. Боли в верхней половине живота, метеоризм, расстройства пищеварения (отрыжка, изжога, тяжесть в животе и т.д.), спленомегалия и гепатомегалия (увеличение печени).
III стадия — выраженная
Присутствуют все признаки и симптомы портальной гипертензии в резко выраженной форме.
IV стадия — стадия осложнений
Развивается напряженный асцит, плохо поддающийся терапии, повторяющиеся кровотечения, а также возможные осложнения.
Осложнения
Основные осложнения: желудочно-кишечные кровотечения, асцит и печеночная энцефалопатия (печеночная недостаточность, комплекс психических, нервных и мышечных нарушений).
Спленомегалия часто вызывает анемию, низкие показатели лейкоцитов и низкие показатели тромбоцитов.
Общими осложнениями, связанными с портальной гипертензией, являются аспирационная пневмония, сепсис, почечная недостаточность, кардиомиопатия, аритмии и гипотония.
Портальная гипертензия является опасным заболеванием, поскольку может вызвать кровотечение. Во многих случаях эпизоды кровотечения считаются неотложными медицинскими ситуациями, потому что смертность от варикозных кровотечений составляет около 50%. Варикоз пищевода очень распространен у людей с прогрессирующим циррозом, и считается, что у каждого из трех человек с варикозом развивается кровотечение.
Прогноз
Портальная гипертензия является осложнением основного заболевания печени. Это заболевание часто можно контролировать, а выживаемость зависит от сохранения функций печени. Чем хуже печень выполняет свои функции, тем хуже прогноз.
Более высокие показатели смертности и заболеваемости у пациентов с тяжелым и стойким желудочно-кишечным кровотечением. Смертность пациентов с диагнозом варикозного расширения вен пищевода составляет 30%.
Пациенты, которые имели хотя бы один эпизод кровотечения из-за варикоза пищевода, имеют 80% шансов повторного кровотечения в течение 1 года. У пациентов с варикозом пищевода осложнения иммунных, сердечно-сосудистых и легочных систем способствуют примерно 20-45% смертей.
Преимущества лечения в клинике
Диагностика
Когда кровь не может легко протекать через печень, она пытается обойти портальную систему, используя венозную систему, чтобы вернуться к сердцу. Возникают осложнения, связанные со снижением кровотока через печень и повышенным давлением внутри вен, что приводит к расширению вен. Варикоз может возникать в пищеводе, желудке и прямой кишке.
Когда кровь пытается найти другой путь к сердцу, открываются новые кровеносные сосуды. Среди них те, которые проходят вдоль стенки верхней части желудка и нижнего конца пищевода. Эти вены могут кровоточить. Кровотечение может быть мягким, в этом случае анемия является наиболее распространенным симптомом; либо серьезным, сопровождающееся кровавой рвотой или меленой (черным, смолистым стулом, который появляется из-за кровотечения из верхних отделов желудочно-кишечного тракта). Варикоз пищевода и желудка может привести к кровотечениям, угрожающим жизни.
Брюшная водянка — избыточное скопление жидкости внутри брюшины, обусловленное сочетанием факторов, включая повышенное давление в портальной системе, застой крови и уменьшение уровня белка в крови. Асцит может достигать огромных размеров, сдавливая диафрагму и мешая нормальному дыханию.
Обратимое расстройство нервной и психической деятельности при заболеваниях печени. Проявляется спутанностью сознания, раздражительностью и сонливостью из-за накопления токсических веществ из-за неспособность печени адекватно фильтровать их.
Увеличение селезенки основной симптом при внепеченочной гипертензии, часто сопровождается анемией и тромбоцитопенией (низким уровнем тромбоцитов в кровотоке).
Снижение количества лейкоцитов в крови увеличивает риск инфицирования. Спонтанный бактериальный перитонит наиболее частое инфекционное заболевание, сопровождающее цирроз и печеночную гипертензию. Сопровождается ознобом, лихорадкой и болью в животе.
Портальная гипертензия является опасным осложнением многих заболеваний печени и несет значительные риски для жизни. Диагностика данного заболевания основана на клинических данных, результатах ультразвуковых и эндоскопических исследований желудка.
Лабораторные исследования позволяют оценить функцию печени и почек, что влияет на прогноз заболевания. С целью подготовки к возможному вмешательству при портальной гипертензии используются методы визуализации сосудов воротной системы. Нами используются методы компьютерной томографии и магнито-резонансной диагностики вен брюшной полости.
В клинике применяются следующие диагностические методы:
Лечение
Лечение портальной гипертензии представляет собой сложную задачу. Сложность связана с тем, что развивающаяся печеночная недостаточность обуславливает плохую переносимость тяжелых сосудистых вмешательств. Однако в нашей клинике отработали технологии лечения портальной гипертензии с низким риском для жизни пациента.
Операции по поводу кровотечений из вен портальной системы
Специальный двухкомпонентный зонд позволяет плотно сжать верхний отдел желудка и нижний отдел пищевода, придавив расширенные вены. Наряду с другими мероприятиями (переливанием плазмы, крови и гемостатических препаратов) позволяет остановить тяжелое желудочно-кишечное кровотечение. Остановка кровотечения не устраняет его причины, поэтому неизбежен рецидив. Но использование этого зонда позволяет отложить вмешательство на портальной системе на более спокойный период и провести его в плановом порядке. Держать зонд в раздутом состоянии рекомендуется не более 6 часов, после чего распускать его на час. Общая продолжительность использования не должна превышать более 2 суток.
Эндоваскулярная технология остановки кровотечения из варикозно-расширенных вен пищевода. Редко выполняется как самостоятельное вмешательство, так как требует чреспеченочного доступа, однако применяется совместно с созданием транспеченочного портокавального анастомоза (TIPS). В просвет варикозно-расширенных вен вводятся спирали и микроэмболы, которые блокируют кровоток в кровоточащих сосудах и способствуют остановке кровотечения.
Современный высокотехнологичный метод лечения портальной гипертензии, применяемый в экстренном порядке или как подготовка к пересадке печени. Смысл вмешательства заключается в создании искусственного соустья между ветвями воротной вены в толще печени и печеночной веной из системы нижней полой. В результате улучшается отток из воротной системы и снижается давления в варикозно-расширенных венах пищевода. Кровотечение быстро останавливается.
Варикозное расширение вены пищевода
Автор материала
Профессор Капранов С.А. — Доктор медицинских наук, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине, за 30 лет личного опыта провел более чем 10 000 различных эндоваскулярных операций
В центре эндоваскулярной хирургии профессора Капранова проводится управляемая эмболизация при варикозном расширении вен. Для вмешательства применяются специальные отделяемые спирали. Благодаря им расширение вен пищевода устраняется в кратчайшие сроки. Вы сможете самостоятельно выбрать клинику для проведения операции.
Варикозное расширение вен пищевода: особенности патологии
Варикозное расширение вен пищевода является достаточно опасной патологией. Она представляет собой деформацию сосудов. В результате развития заболевания увеличивается просвет вен, выделяются их стенки и образуются узлы. Деформированные сосуды становятся очень извитыми и достаточно рыхлыми. Слизистая оболочка, которая располагается над сосудами, подвергается повреждениям и воспалениям.
Заболевание опасно еще и отсутствием симптомов на раннем этапе развития. На начальных стадиях варикозное расширение вен не проявляет себя никакими признаками. По этой причине человек и не догадывается о том, что в его организме происходят патологические процессы. Между тем варикозное расширение очень опасно!
При развитии варикозного расширения вен пациент жалуется на:
Нередко варикозному заболеванию пищевода сопутствует эзофагит. Этот процесс является воспалительным.
Опасным осложнением при патологии становится кровотечение. В результате появляется слабость и одышка. Ухудшается общее состояние здоровья. Пациент может страдать от потери веса.
Как диагностируется заболевание?
Варикозное расширение вен пищевода диагностируется путем:
Как проводится лечение варикоза пищевода?
Основной целью терапии при варикозном расширении вен пищевода является профилактика кровотечения. В некоторых случаях специалистам приходится устранять и последствия уже перенесенных кровотечений.
Расширение вен лечится путем назначения:
В некоторых случаях осуществляется введение специальных коллоидных растворов. Также проводятся переливания плазмы, крови и эритроцитарной массы.
К операциям на пищеводе прибегают тогда, когда медикаментозная терапия не дает желаемого результата.
Все вмешательства делятся на 2 группы:
Эндоскопические вмешательства на пищеводе проводятся путем:
Хирургические операции по предупреждению кровотечений в результате расширений вен пищевода проводятся путем:
Все операции на венах пищевода являются достаточно опасными. Кроме того, варикозные патологии с их помощью невозможно устранить полностью. Нередко возникают рецидивы, а операции провоцируют риски ряда осложнений.
Именно поэтому с варикозными патологиями сегодня борются с применением еще одного метода. Он является инновационным и позволяет забыть о проблеме!
Эмболизация при расширенных венах не напрасно пользуется популярностью!
Основные особенности вмешательства!
К достоинствам эмболизации вены относят:
Какие рекомендации дают пациентам врачи?
Какой образ жизни вести после эмболизации сосудов пищевода?
Запрещено принимать слишком горячую и холодную пищу. Это может привести к повреждению пищевода и его вен.
Основные достоинства метода эмболизации вен, применяемого в центре профессора Капранова
Эндоваскулярная эмболизация в нашем центре представляет собой малотравматичную процедуру. Она кардинально отличается от стандартных хирургических вмешательств отсутствием больших разрезов на вене и тканях. Кроме того, при эмболизации не требуется вводить пациента в общий наркоз. Это снижает многочисленные риски, делает вмешательство возможным при наличии общих противопоказаний к стандартной операции.
К достоинствам проведения вмешательства в центре профессора Капранова также относят:
От чего зависит стоимость эмболизации вен пищевода?
Окончательная стоимость эмболизации сосудов пищевода во многом определяется такими факторами, как:
Таким образом, стоимость процедуры зависит от ряда факторов, не имеющих прямого отношения к качеству предоставления медицинских услуг. Благодаря этому даже при относительно небольших затратах вы можете рассчитывать на получение квалифицированной профессиональной поддержки.
Ориентировочные расценки представлены на сайте нашего центра.
Звоните в клиники, в которых лечение пищевода проводится профессором Капрановым, задавайте свои вопросы.
Также вы можете связаться с профессионалом, воспользовавшись его личными телефонами:
С профессором Капрановым можно обсудить все особенности лечения пищевода. Вы сможете оговорить все тонкости вмешательства и запланировать первый прием и обследование. Операция может быть проведена уже в ближайшее время.
Что такое эмболизация вен пищевода
Портальная гипертензия (ПГ) – один из ведущих синдромов, характерных для цирроза печени (ЦП) [1]. При ПГ в круг патологических расстройств вовлекается сосудистое русло всех органов брюшной полости. Для данного осложнения характерны следующие проявления: пищеводно-желудочное кровотечение из варикозно расширенных вен (ВРВ) пищевода и желудка, асцит, гепато-ренальный синдром, энцефалопатия, спонтанный бактериальный перитонит [3, 6, 8]. Наиболее опасное и нередко фатальное для больного осложнение – варикозное кровотечение [4, 10].
Основные сосудистые коллекторы, в области которых чаще всего происходят такие геморрагии, располагаются в кардио-эзофагеальной зоне, а именно в нижней трети пищевода и кардиального отдела желудка. Именно здесь при ПГ формируется один из самых клинически значимых порто-кавальных анастомозов между левой желудочной веной (ЛЖВ), являющейся ветвью воротной вены (ВВ) и непарной и полунепарной венами, несущими кровь в верхнюю полую вену [2, 12].
Существует множество медикаментозных, эндоскопических и хирургических методов гемостаза при варикозных кровотечениях. Однако, несмотря на это, результаты лечения подобных пациентов в большинстве случаев остаются неудовлетворительными [9, 11]. Операция трансъюгулярного внутрипеченочного портосистемного шунтирования (TIPS/ТИПС) нашла широкое применение в клинической практике в лечении ПГ с целью остановки и профилактики рецидивов кровотечений из ВРВ пищевода и желудка ввиду миниинвазивности, отсутствия широкого хирургического доступа и многочасового анестезиологического пособия, которые могут усугубить течение фонового заболевания и смерти пациента [5, 7]. Известна разновидность выполнения TIPS/ТИПС с последующей эмболизацией ЛЖВ и пищеводных вен. После установки внутрипеченочного стента через созданный портосистемный шунт в ЛЖВ проводят ангиографический катетер и устанавливают эмболизационные спирали, тем самым редуцируя кровоток в пищеводных вариксах. Данная манипуляция приводит к снижению риска рецидива пищеводного кровотечения в случае дисфункции внутрипеченочного шунта [9].
Проведя анализ литературных данных, следует сказать, что эндоваскулярная эмболизация ЛЖВ является эффективной дополнительной манипуляцией к портосистемному шунтирующему вмешательству в лечении и профилактике варикозных пищеводно-желудочных кровотечений. Успех выполнения данного оперативного пособия зависит от особенностей анатомического строения системы ВВ и в частности ЛЖВ.
Цель исследования – оценить эффективность выполнения операции TIPS/ТИПС в сочетании с селективной эмболизацией ЛЖВ в лечении и профилактике варикозных пищеводно-желудочных кровотечений при ПГ путем клинико-анатомического обоснования данной манипуляции.
Материалы и методы исследования
Материалом для исследования послужили данные, полученные при анализе клинических, ультразвуковых, томографических и ангиографических данных. В хирургической клинике РостГМУ в период с 2007 по 2014 гг. операции TIPS/ТИПС подверглись 144 пациента с ПГ цирротического генеза. Отметим, что 102 пациентам основным показанием к оперативному вмешательству стали продолжающиеся или состоявшиеся в недавнем анамнезе пищеводно-желудочные кровотечения. В 52 случаях данное вмешательство дополнено селективной эмболизацией ЛЖВ. С целью оценки эффективности выполнения эмболизации ЛЖВ и обоснованности ее применения в профилактике варикозных кровотечений проведен ретроспективный анализ клинических случаев. Сформированы 2 сопоставимые клинические группы путем случайной выборки из общего количества больных. В каждую группу вошли по 35 больных. Больным I группы выполняли операцию TIPS/ТИПС, во II – основной этап оперативного пособия дополняли селективной эмболизацией ЛЖВ. Возраст больных – от 27 до 74 лет (в среднем 47,9 ± 6,8). Распределение больных в выборке по степени тяжести печеночной недостаточности в соответствии с критериями Чайлд-Пью было следующим: 3 человека относились к классу А, 35 – к классу В, 32 – к классу С. Отметим, что группы были сопоставимы по полу и возрасту, а также по количеству больных в зависимости от класса хронической печеночной недостаточности. Как видно, большинство больных обеих групп находились в суб- и декомпенсированных стадиях заболевания. В предоперационном периоде наряду с рутинными методами обследования всем больным выполнялось дуплексное сканирование системы ВВ и селезеночной вены для определения их диаметра, линейной, объемной скоростей кровотока, его характера. С целью оптимизации прогноза проведения TIPS/ТИПС в контексте предстоящего вмешательства и оценки внутрипаренхиматозного топографоанатомического расположения браншей ВВ, визуализации внепеченочных ветвей спленопортального ствола у больных с ЦП выполнялась компьютерная спленопортография. Также оценивались анатомические особенности ЛЖВ. Основными показаниями для выполнения эмболизации явились наличие пищеводных кровотечений в анамнезе, рентген-ангиографическое подтверждение варикозно расширенных вен (ВРВ) пищевода. Обязательным завершающим этапом хирургического пособия являлась контрольная прямая портография. Критерием адекватного выполненного вмешательства было контрастирование ВВ, внутрипеченочного стента без дефектов наполнения, а также отсутствие кровотока по ранее выявленным ВРВ пищевода.
Результаты исследования и их обсуждение
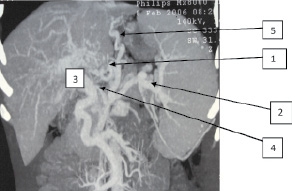
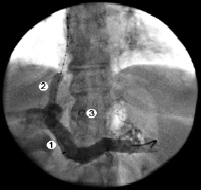
Правильная оценка рентген-анатомических особенностей ВВ и ее внутрипеченочных ветвлений в контексте предстоящей операции TIPS/ТИПС является залогом успешного создания внутрипеченочного канала с целью эффективной декомпрессии портальной системы. Весьма информативную картину представления о состоянии сплено-портального русла и особенностей анатомии ЛЖВ на дооперационном этапе дает компьютерная сплено-портография (рис. 1).
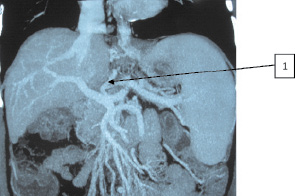
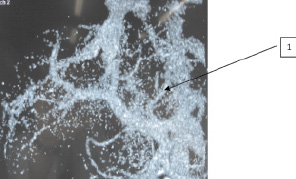
Во всех случаях было выявлено, что при ПГ в первую очередь расширяются сосуды, расположенные ближе к воротам печени. Такими сосудами являются ЛЖВ, селезеночная и мезентериальные вены. Объясняется это тем, что развивающийся гепатофугальный кровоток всегда идет по пути наименьшего сопротивления. Кроме этого, визуализировались расширенные порто-кавальные анастомозы области ворот печени и селезенки. У больных обеих групп отмечено расширение ЛЖВ (1) и извитые пищеводные вены (5) (рис. 1). В нескольких случаях контрастировались расширенные и варикозно-трансформированные венозные стволы выше диафрагмы, впадающие в систему непарной и полунепарной вен (пути оттока в систему верхней полой вены) (рис. 2). В ряде случаев для более детальной оценки анатомического строения системы ВВ и в частности ЛЖВ нами использовалась 3D-реконструкция изображения (рис. 3). Отметим, что ВРВ пищевода у пациентов визуализировались при выполнении эзофагогастродуоденоскопии (ЭГДС).
Рис. 1. Пациентка Л., 45 лет. СКТ-ангиография: 1 – варикозно трансформированная ЛЖВ; 2 – селезеночная вена; 3 – ВВ; 4 – устье впадения ЛЖВ в ВВ; 5 – нижние пищеводные вены
Рис. 2. Пациентка К., 54 лет. СКТ-ангиография. 1 – ЛЖВ
Рис. 3. Пациентка К., 54 лет. СКТ-ангиография, 3D-реконструкция. 1 – ЛЖВ
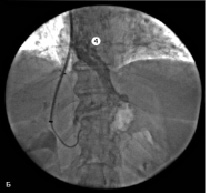
Во всех случаях II группы наблюдения этап эмболизации стал дополнением основному эндоваскулярному хирургическому мероприятию. Основными показаниями к данной манипуляции служили пищеводно-желудочные кровотечения в анамнезе и возможность технического исполнения. Непосредственно перед оперативным пособием для визуализации анатомических особенностей порто-печеночного русла применялась селективная ангиография данных венозных сосудов. После установки внутрипеченочного стента выполнялась контрольная прямая портография. Помимо оценки функционирования внутрипеченочного шунта, мы обращали внимание на наличие ВРВ пищевода и варикозно трансформированной ЛЖВ (рис. 4).
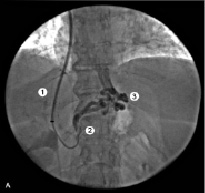
Рис. 4. Пациентка Д., 35 лет: 1 – стент; 2 – левая желудочная вена; 3, 4 – варикозно расширенные вены
Рис. 5. Пациентка Д., 35 лет: 1 – ВВ; 2 – TIPS/ТИПС; 3 – спираль Gianturco
У двух больных ЛЖВ была представлена несколькими стволами. В подобных случаях мы раздельно катетеризировали каждый из варикозных стволов с последующей эмболизацией.
Как видно, процедуру эмболизации ЛЖВ, дополняющую шунтирование системы ВВ, мы выполнили в 36,1 % случаев от общего количества больных. У пациентов I группы селективная эмболизация ЛЖВ в ряде случаев не выполнялась. Техническая невозможность исполнения данной манипуляции даже при рентгенологически подтвержденной картине наличия ВРВ пищевода объяснялась зависимостью от анатомических особенностей ЛЖВ и угла отхождения ее ствола ВВ. Наличие острого угла α (угол между ВВ и ЛЖВ) в 30° и менее представляло технические трудности в селективной катетеризации ЛЖВ либо вен пищевода с помощью катетера диаметром 5–6 F типа Cobra. Наличие выраженных ВРВ пищевода более 15 мм в диаметре также не являлось показанием к селективной эмболизации ЛЖВ. Объясняется это тем, что сброс портальной крови в нижнюю пищеводную вену происходил не только через ЛЖВ, но и через селезеночную вену, далее в левую желудочно-сальниковую, короткие желудочные вены, вены подслизистого слоя тела и дна желудка и далее в пищеводные. В подобных случаях пищеводные вены имели несколько венозных притоков. Кроме этого, наличие большего диаметра расширенных вен является предрасполагающим фактором к миграции эмболизационных спиралей.
Проанализировав полученные данные, мы установили следующие показания к селективной эмболизации ЛЖВ, дополняющей операцию портосистемного шунтирования:
На основании проведенного ретроспективного анализа отмечено следующее. Селективная эмболизация ЛЖВ, выполняемая через созданный портосистемный канал, является эндоваскулярной процедурой, имеющей целью устранить ретроградный кровоток по венозной магистрали, соединяющей ВВ с сосудами, располагающимися в подслизистом слое нижней трети пищевода и кардиального отдела желудка. Сочетание двух этапов оперативного пособия, а именно TIPS/ТИПС и селективной эмболизации ЛЖВ, позволяет редуцировать ретроградный гепатофугальный кровоток в ВВ и сброс крови в гастроэзофагеальный бассейн, что в значительной мере снижает риск рецидива пищеводно-желудочного кровотечения даже в условиях тромбоза стента.
Тем не менее, по данным некоторых авторов, эндоваскулярная эмболизация ЛЖВ усложняет оперативное вмешательство и увеличивает время его продолжительности, что негативно может сказываться на течении основного заболевания в послеоперационном периоде [9]. Более того, с течением времени существует вероятность снижения эффективности данной манипуляции вследствие вариабельности коллатерального портального кровообращения при рецидиве ПГ [1].
Приводим результаты наблюдения по истечению 3-летнего периода. Дисфункция созданного портосистемного шунта выявлена в послеоперационном периоде у 14 больных I группы и у 12 – во II. В первой группе наблюдений рецидивы варикозных пищеводных кровотечений зарегистрированы у 12 пациентов. 360-дневная летальность составила 20 % (7 человек). Что касается второй группы больных, отметим, что в сроки от одного месяца до одного года тромбоз шунта проявился рецидивом пищеводного кровотечения у 2 пациентов (5,7 %), а на протяжении всего исследования у остальных 10 больных тромбоз шунта стал случайной находкой при плановом ультразвуковом исследовании, которому с определенной периодичностью подвергаем всех оперированных. Все 10 больных, у которых тромбоз шунта протекал без клинической манифестации пищеводных геморрагий, подверглись эмболизации ЛЖВ в дополнение к формированию TIPS/ТИПС. 360-дневная летальность в этой группе пациентов составила 11,4 % (4 человека), причем 3 из них умерло от декомпенсации основного заболевания без клинико-лабораторных признаков пищеводно-желудочного кровотечения. Трехлетняя выживаемость пациентов I группы составила 57,1 % (20 больных), во II – 68,6 % (24 пациента). Основная причина летальности больных II – декомпенсация основного заболевания с развитием тяжелых форм печеночной энцефалопатии и гепато-ренального синдрома 1 типа. Таким образом, несмотря на техническую сложность манипуляции эмболизации ЛЖВ и, как следствие, удлинение времени оперативного пособия, нам удалось снизить летальность и повысить выживаемость больных во второй группе наблюдений.
В заключение необходимо отметить следующее. Соблюдение сформулированных показаний, техническую возможность исполнения селективной эмболизации ЛЖВ позволяет надежно профилактировать пищеводно-желудочные кровотечения даже в условиях тромбированного внутрипеченочного шунта. Это позволяет не только снизить рецидив варикозных кровотечений портального генеза в отдаленном послеоперационном периоде и летальность, но и повысить выживаемость данной категории больных.
Выводы
Рецензенты:
Черкасов М.Ф., д.м.н., профессор, главный хирург ЮФО, заведующий кафедрой хирургических болезней ФПК и ППС ГБОУ ВПО РостГМУ Минздрава России, г. Ростов-на-Дону;
Шапошников А.В., д.м.н., профессор, ФГБУ «РНИОИ» Минздрава России, главный научный сотрудник центра подготовки и переподготовки специалистов, г. Ростов-на-Дону.
 Причины и факторы риска
Причины и факторы риска