можно ли пить вальдоксан днем
Вальдоксан ® (Valdoxan ® )
таб., покр. пленочной обол., 25 мг: 14, 28, 98 или 100 шт. Рег. №: ЛСР-000540/08
Клинико-фармакологическая группа:
Форма выпуска, состав и упаковка
Таблетки, покрытые пленочной оболочкой оранжево-желтого цвета, продолговатые, с изображением логотипа фирмы голубого цвета на одной стороне.
Описание активных компонентов препарата «Вальдоксан ® »
Фармакологическое действие
Агомелатин активен на валидированных моделях депрессии (тест приобретенной беспомощности, тест отчаяния, хронический стресс умеренной выраженности), равно как и на моделях с десинхронизацией циркадных ритмов, а также в экспериментальных ситуациях тревоги и стресса. Показано, что агомелатин не влияет на захват моноаминов и не имеет сродства к α-, β-адренорецепторам, гистаминовым рецепторам, холинорецепторам, допаминовым и бензодиазепиновым рецепторам.
Агомелатин усиливает высвобождение допамина и норадреналина, в особенности в области префронтальной коры мозга и не влияет на концентрацию внеклеточного серотонина. В экспериментальных исследованиях на животных со смоделированной десинхронизацией циркадных ритмов было показано, что агомелатин восстанавливает синхронизацию циркадных ритмов через стимуляцию мелатониновых рецепторов.
Агомелатин способствует восстановлению нормальной структуры сна, снижению температуры тела и выделению мелатонина.
Показана эффективность краткосрочного применения агомелатина (терапия 6-8 недель) в дозах 25-50 мг у пациентов с большими депрессивными эпизодами.
Также показана эффективность применения агомелатина у больных с более тяжелыми формами депрессивного расстройства (оценка по шкале Гамильтона ≥ 25).
Агомелатин был также эффективен при изначально высоких уровнях тревоги, равно как и при сочетании тревожных и депрессивных расстройств.
Агомелатин не оказывает отрицательного воздействия на внимательность и память, у пациентов с депрессией агомелатин в дозе 25 мг увеличивает продолжительность фазы медленного сна без изменения количества и продолжительности фаз быстрого сна. Прием агомелатина в дозе 25 мг также способствует более быстрому наступлению сна со снижением ЧСС и улучшению качества сна (начиная с первой недели лечения); при этом заторможенности в дневное время не отмечается.
На фоне приема агомелатина отмечена тенденция к снижению частоты сексуальной дисфункции (влияние на возбуждение и оргазм).
Прием агомелатина не оказывает влияния на ЧСС и АД, не вызывает сексуальных нарушений, не вызывает синдрома отмены (даже при резком прекращении лечения) и синдрома привыкания.
Показания
— лечение большого депрессивного расстройства у взрослых.
Режим дозирования
Препарат назначают внутрь.
Рекомендуется контролировать функцию печени в начале терапии и затем периодически, через 3 недели, через 6 недель (окончание купирующего периода терапии), 12 недель и 24 недели (окончание поддерживающего периода терапии) после начала терапии, и в дальнейшем в соответствии с клинической ситуацией. При увеличении дозы следует контролировать функцию печени с той же частотой, что и в начале применения препарата.
Лекарственную терапию депрессий следует проводить, по крайней мере, в течение 6 мес для полного прекращения симптомов.
В случае прекращения лечения нет необходимости в постепенном снижении дозы.
Вальдоксан ® можно принимать независимо от приема пищи. Таблетки следует проглатывать целиком, не разжевывая.
Для улучшения контроля приема препарата на блистере, содержащем таблетки, отпечатан календарь.
Побочное действие
В клинических исследованиях Вальдоксан ® получали более 7200 пациентов с депрессией. Побочные эффекты чаще всего были незначительно или умеренно выражены и наблюдались в первые 2 недели лечения. Наиболее часто отмечались тошнота и головокружение. Отмеченные побочные действия, как правило, были преходящими и, в основном, не требовали прекращения лечения. В ряде случаев сложно разграничить симптомы депрессивного расстройства и побочные эффекты терапии агомелатином.
Противопоказания
— печеночная недостаточность (например, цирроз или заболевание печени в активной фазе);
— одновременное применение сильных ингибиторов изофермента CYP1A2 (таких как флувоксамин, ципрофлоксацин);
— детский возраст до 18 лет (из-за отсутствия достаточного опыта клинического применения). У детей и подростков на фоне приема других антидепрессантов суицидальное поведение (попытки суицида и суицидальные мысли) и враждебность (преимущественно агрессивность, конфликтное поведение, раздражение) отмечались чаще по сравнению с группой плацебо;
— непереносимость лактозы (лактазная недостаточность, галактоземия и синдром мальабсорбции глюкозы/галактозы);
— повышенная чувствительность к агомелатину и/или любому из вспомогательных веществ препарата.
С осторожностью следует назначать препарат пациентам пожилого возраста (65 лет и старше); при больших депрессивных эпизодах у пациентов с умеренной и выраженной почечной недостаточностью; при одновременном назначении агомелатина с умеренными ингибиторами изофермента CYP1A2 (такими как пропранолол, грепафлоксацин, эноксацин); пациентам с маниакальными или гипоманиакальными эпизодами в анамнезе, пациентам, в анамнезе которых имелись события, связанные с суицидом, а также пациентам, имевшим суицидальные намерения до начала терапии; при лечении больших депрессивных эпизодов у пожилых пациентов с деменцией (из-за отсутствия данных об эффективности и безопасности применения препарата у данной группы пациентов).
Следует соблюдать осторожность при назначении препарата пациентам, употребляющим алкоголь в значительных количествах или принимающим препараты, способные вызвать нарушение функции печени.
Беременность и лактация
Данные о применении агомелатина при беременности отсутствуют или ограничены (менее 300 исходов беременности).
Исследования на животных не выявили прямых или опосредованных вредных воздействий на течение беременности, развитие эмбриона и плода, родовую деятельность и постнатальное развитие. При назначении препарата беременным следует соблюдать осторожность.
Неизвестно, проникает ли агомелатин в грудное молоко у женщин в период лактации. В экспериментальных исследованиях на животных было показано, что агомелатин и его метаболиты проникают в грудное молоко. Если лечение агомелатином необходимо, грудное вскармливание следует прекратить.
Применение при нарушениях функции печени
Препарат противопоказан при тяжелой печеночная недостаточности. Пациентам с легкой и умеренной степенью печеночной недостаточности препарат рекомендуется назначать в суточной дозе 25 мг (1 таб.).
Применение при нарушениях функции почек
Пациентам с почечной недостаточностью коррекция дозы не требуется.
Особые указания
Мониторинг показателей функции печени
Рекомендуется контролировать функцию печени в начале терапии и затем периодически, через 3 недели, через 6 недель (окончание купирующего периода терапии), 12 недель и 24 недели (окончание поддерживающего периода терапии) после начала терапии, и в дальнейшем в соответствии с клинической ситуацией. При увеличении дозы следует контролировать функцию печени с той же частотой, что и в начале применения препарата.
При повышении активности трансаминаз в сыворотке крови следует провести повторное исследование в течение 48 ч. Если активность трансаминаз более чем в 3 раза превышает ВГН, прием препарата следует прекратить. В дальнейшем следует регулярно контролировать функциональное состояние печени до нормализации активности трансаминаз.
При проявлении симптомов и признаков возможных нарушений функции печени (таких как темная моча, обесцвеченный стул, желтизна кожи/глаз, боль в правой верхней части живота, недавно появившаяся постоянная и необъяснимая утомляемость) прием Вальдоксана следует немедленно прекратить.
Следует соблюдать осторожность при назначении препарата Вальдоксан ® пациентам с повышенной активностью трансаминаз до начала терапии (выше ВГН, но не более чем в 3 раза относительно ВГН).
Следует соблюдать осторожность при назначении препарата Вальдоксан ® пациентам с факторами риска развития нарушений функции печени, такими как ожирение/избыточная масса тела/неалкогольный жировой гепатоз, сахарный диабет, употребление алкоголя в значительных количествах или прием препаратов, способных вызывать нарушение функции печени.
Пациенты пожилого возраста
Эффективность применения препарата у пожилых пациентов (в возрасте 65 лет и старше) не установлена. Имеются ограниченные данные о применении препарата Вальдоксан ® при больших депрессивных эпизодах у пациентов в возрасте 65 лет и старше. При назначении препарата пациентам пожилого возраста следует соблюдать осторожность.
Пациенты с почечной недостаточностью
У пациентов с почечной недостаточностью тяжелой степени значимого изменения фармакокинетических параметров не отмечалось. Однако опыт применения препарата при больших депрессивных эпизодах у пациентов с умеренной или выраженной почечной недостаточностью ограничен. При назначении препарата Вальдоксан ® таким пациентам следует соблюдать осторожность.
Следует соблюдать осторожность при применении препарата Вальдоксан ® у пациентов с биполярными расстройствами, маниакальными или гипоманиакальными эпизодами в анамнезе. При появлении симптомов мании следует прекратить прием препарата.
При депрессивном состоянии повышен риск суицидальных мыслей, самоповреждений и суицида (событий, связанных с суицидом). Риск сохраняется до наступления отчетливой ремиссии. Пациенты должны находиться под медицинским наблюдением вплоть до улучшения состояния (после начала терапии может пройти несколько недель, прежде чем состояние улучшится). Клинический опыт свидетельствует, что риск суицида может увеличиваться на ранних этапах наступления ремиссии.
Пациенты, в анамнезе которых имелись события, связанные с суицидом, а также пациенты, имевшие суицидальные намерения до начала терапии, относятся к группе риска и во время проведения терапии должны находиться под пристальным медицинским наблюдением.
Результаты мета-анализа клинических исследований антидепрессантов у пациентов с психическими расстройствами свидетельствуют о повышенном риске суицидального поведения у пациентов в возрасте до 25 лет на фоне приема антидепрессантов по сравнению с плацебо.
В период лечения пациенты, особенно относящиеся к группе риска, должны находиться под пристальным медицинским наблюдением, особенно в начале терапии и при изменении дозы препарата. Пациенты (и лица, осуществляющие уход за ними) должны быть информированы о необходимости немедленного обращения к врачу при ухудшении состояния, суицидальном и необычном поведении, а также при появлении суицидальных мыслей.
Совместное применение с ингибиторами изофермента CYP1A2
Следует соблюдать осторожность при одновременном применении агомелатина с умеренными ингибиторами изофермента CYP1А2 (такими как пропранолол, грепафлоксацин, эноксацин) из-за возможности повышения концентрации агомелатина.
Влияние на способность к вождению автотранспорта и управлению механизмами
Передозировка
Данные о передозировке агомелатина ограничены.
Симптомы: сонливость, боль в эпигастрии, беспокойство, слабость, тревога, ажитация, напряжение, головокружение, цианоз, недомогание. При приеме пациентом агомелатина в дозе 2450 мг состояние нормализовалось самостоятельно, без нарушений со стороны сердечно-сосудистой системы или изменения лабораторных показателей.
Лечение: специфический антидот для агомелатина не известен. Проводят симптоматическое лечение и мониторинг в специализированных отделениях с последующим наблюдением.
Лекарственное взаимодействие
Потенциально возможное взаимодействие
Флувоксамин, является сильным ингибитором изофермента CYP1A2 и умеренным ингибитором изофермента CYP2C9 и существенно замедляет метаболизм агомелатина, при этом концентрация агомелатина увеличивается примерно в 60 (12-412) раз. Поэтому одновременное применение агомелатина и сильных ингибиторов изофермента CYP1A2 (таких как флувоксамин, ципрофлоксацин) противопоказано.
Одновременное назначение агомелатина и эстрогенов, которые являются умеренными ингибиторами изофермента CYP1A2, приводит к увеличению концентрации агомелатина в несколько раз. Хотя комбинированное применение агомелатина и эстрогенов не сопровождалось ухудшением профиля безопасности проводимой терапии, следует соблюдать осторожность при одновременном назначении агомелатина с другими умеренными ингибиторами изофермента CYP1A2 (такими как пропранолол, грепафлоксацин, эноксацин) до накопления достаточного клинического опыта.
Рифампицин, как индуктор обоих изоферментов цитохрома P450, участвующих в метаболизме агомелатина, способен уменьшать биодоступность агомелатина. Показано, что курение, индуцируя изофермент CYP1A2, уменьшает биодоступность агомелатина, особенно у пациентов, злоупотребляющих курением (более 15 сигарет/день).
Вероятность действия агомелатина на другие лекарственные препараты
In vivo агомелатин не индуцирует изоферменты цитохрома Р450. Агомелатин не ингибирует изофермент CYP1A2 in vivo и другие изоферменты цитохрома Р450 in vitro. Поэтому агомелатин не влияет на концентрацию лекарственных средств, метаболизм которых связан с этими изоферментами.
Агомелатин не изменяет свободную концентрацию препаратов, которые в значительной степени связываются с белками плазмы и, в свою очередь, они не влияют на концентрацию агомелатина.
Выявлено отсутствие фармакокинетического и фармакодинамического взаимодействия агомелатина и препаратов, часто применяемых в целевой популяции пациентов: бензодиазепинов, препаратов лития, пароксетина, флуконазола и теофиллина.
Не рекомендуется применение агомелатина совместно с алкоголем.
Отсутствуют данные о применении агомелатина одновременно с электросудорожной терапией (ЭСТ). Поскольку в опытах на животных агомелатин не способствовал возникновению судорог, нежелательные последствия совместного использования агомелатина и ЭСТ представляются маловероятными.
Условия отпуска из аптек
Препарат отпускается по рецепту.
Условия и сроки хранения
Лекарственное взаимодействие
Потенциально возможное взаимодействие
Флувоксамин, является сильным ингибитором изофермента CYP1A2 и умеренным ингибитором изофермента CYP2C9 и существенно замедляет метаболизм агомелатина, при этом концентрация агомелатина увеличивается примерно в 60 (12-412) раз. Поэтому одновременное применение агомелатина и сильных ингибиторов изофермента CYP1A2 (таких как флувоксамин, ципрофлоксацин) противопоказано.
Одновременное назначение агомелатина и эстрогенов, которые являются умеренными ингибиторами изофермента CYP1A2, приводит к увеличению концентрации агомелатина в несколько раз. Хотя комбинированное применение агомелатина и эстрогенов не сопровождалось ухудшением профиля безопасности проводимой терапии, следует соблюдать осторожность при одновременном назначении агомелатина с другими умеренными ингибиторами изофермента CYP1A2 (такими как пропранолол, грепафлоксацин, эноксацин) до накопления достаточного клинического опыта.
Рифампицин, как индуктор обоих изоферментов цитохрома P450, участвующих в метаболизме агомелатина, способен уменьшать биодоступность агомелатина. Показано, что курение, индуцируя изофермент CYP1A2, уменьшает биодоступность агомелатина, особенно у пациентов, злоупотребляющих курением (более 15 сигарет/день).
Вероятность действия агомелатина на другие лекарственные препараты
In vivo агомелатин не индуцирует изоферменты цитохрома Р450. Агомелатин не ингибирует изофермент CYP1A2 in vivo и другие изоферменты цитохрома Р450 in vitro. Поэтому агомелатин не влияет на концентрацию лекарственных средств, метаболизм которых связан с этими изоферментами.
Агомелатин не изменяет свободную концентрацию препаратов, которые в значительной степени связываются с белками плазмы и, в свою очередь, они не влияют на концентрацию агомелатина.
Выявлено отсутствие фармакокинетического и фармакодинамического взаимодействия агомелатина и препаратов, часто применяемых в целевой популяции пациентов: бензодиазепинов, препаратов лития, пароксетина, флуконазола и теофиллина.
Не рекомендуется применение агомелатина совместно с алкоголем.
Отсутствуют данные о применении агомелатина одновременно с электросудорожной терапией (ЭСТ). Поскольку в опытах на животных агомелатин не способствовал возникновению судорог, нежелательные последствия совместного использования агомелатина и ЭСТ представляются маловероятными.
Вальдоксан (Агомелатин)
Вальдоксан (Агомелатин)
Клинико-фармакологическая группа
Фармакологическое действие
Антидепрессант, агонист мелатонинергических МТ1— и МТ2-рецепторов и антагонист серотониновых 5-НТ2с-рецепторов.
Агомелатин активен на валидированных моделях депрессии (тест приобретенной беспомощности, тест отчаяния, хронический стресс умеренной выраженности), равно как и на моделях с десинхронизацией циркадных ритмов, а также в экспериментальных ситуациях тревоги и стресса. Показано, что агомелатин не влияет на захват моноаминов и не имеет сродства к α-, β-адренорецепторам, гистаминергическим рецепторам, холинергическим, допаминергическим и бензодиазепиновым рецепторам.
Агомелатин усиливает высвобождение дофамина и норадреналина, в особенности в области префронтальной коры мозга и не влияет на концентрацию внеклеточного серотонина. В опытах на животных с десинхронизацией циркадных ритмов было показано, что агомелатин восстанавливает синхронизацию циркадных ритмов посредством стимуляции мелатониновых рецепторов.
Агомелатин способствует восстановлению нормальной структуры сна, снижению температуры тела и выделению мелатонина.
Показана эффективность краткосрочного применения агомелатина (терапия 6-8 недель) в дозах 25-50 мг у пациентов с большими депрессивными эпизодами.
Также показана эффективность применения агомелатина у пациентов с более тяжелыми формами депрессивного расстройства (оценка по шкале Гамильтона ≥25).
Агомелатин был также эффективен при изначально высоких уровнях тревоги, равно как и при сочетании тревожных и депрессивных расстройств.
Эффективность агомелатина была продемонстрирована в 6 из 7 клинических исследованиях (преимущество (2 исследования) или сопоставимая эффективность (4 исследования)) в гетерогенных популяциях взрослых пациентов с депрессией по сравнению с селективными ингибиторами обратного захвата серотонина (СИОЗС)/селективными ингибиторами обратного захвата норадреналина (СИОЗСН) (сертралин, эсциталопрам, флуоксетин, венлафаксин или дулоксетин). Антидепрессивный эффект оценивался по шкале Гамильтона (17-пунктовая версия) либо как первичная, либо как вторичная конечная точка.
Агомелатин не оказывает отрицательного воздействия на внимательность и память, у пациентов с депрессией агомелатин в дозе 25 мг увеличивает продолжительность фазы медленного сна без изменения количества и продолжительности фаз быстрого сна. Прием агомелатина в дозе 25 мг также способствует более быстрому наступлению сна со снижением ЧСС и улучшению качества сна (начиная с первой недели лечения); при этом заторможенности в дневное время не отмечается.
На фоне приема агомелатина отмечена тенденция к снижению частоты сексуальной дисфункции (влияние на возбуждение и оргазм).
Прием агомелатина не оказывает влияния на ЧСС и АД, не вызывает сексуальных нарушений, не вызывает синдрома отмены (даже при резком прекращении лечения) и синдрома привыкания.
Эффективность агомелатина в дозе 25-50 мг 1 раз/сут подтверждена у пациентов пожилого возраста (моложе 75 лет) с депрессией в ходе 8-недельного клинического исследования. У пациентов в возрасте 75 лет и старше нет подтвержденных данных о наличии существенного эффекта. Переносимость агомелатина у пациентов пожилого возраста сопоставима с таковой у молодых.
В ходе проведения 3-недельного контролируемого исследования с участием пациентов с большим депрессивным расстройством и недостаточным терапевтическим эффектом от приема пароксетина (СИОЗС) или венлафаксина (СИОЗСН), при переходе с терапии данными антидепрессантами на лечение агомелатином наблюдался синдром отмены. Синдром отмены появлялся как после одномоментного прекращения лечения назначенными ранее СИОЗС/СИОЗСН, так и при их постепенной отмене, что могло быть ошибочно принято за проявление низкой эффективности агомелатина на начальном этапе лечения.
Количество пациентов, у которых через неделю после отмены СИОЗС/СИОЗСН наблюдался хотя бы один симптом, связанный с синдромом отмены, было ниже в группе с длительным снижением дозы (постепенное снижение дозы СИОЗС/СИОЗСН в течение 2 недель), чем в группе с быстрым снижением дозы (постепенное снижение дозы СИОЗС/СИОЗСН в течение 1 недели), и чем при одномоментной отмене: 56.1%, 62.6% и 79.8% пациентов соответственно.
Фармакокинетика
После приема внутрь агомелатин быстро (≥80%) всасывается. Cmax в плазме достигается через 1-2 ч после приема внутрь. Абсолютная биодоступность после приема терапевтической дозы низкая (
Вальдоксан (агомелатин): современный подход к лечению умеренных и тяжелых эндогенных депрессий непсихотического уровня
Резюме. Проведена оценка терапевтической эффективности и переносимости Вальдоксана (агомелатина) в дозе 25-50 мг в сутки у 26 больных с умеренными и тяжелыми эндогенными депрессиями непсихотического уровня. Продолжительность исследования составила 56 дней. Редукция депрессивной симптоматики отмечена у всех 26 больных. К завершению исследования формирование ремиссии по шкале депрессии HDRS-21 наблюдалось у 76,9% пациентов. Побочные эффекты препарата выявлены лишь в одном случае, имели слабую степень выраженности, быстро редуцировались, не препятствовали проведению терапии. Результаты исследования показали, что Вальдоксан обладает высокой терапевтической антидепрессивной активностью при лечении больных эндогенными депрессивными состояниями непсихотического уровня умеренной и тяжелой степени выраженности.
Ключевые слова: эндогенная депрессия, депрессия непсихотического уровня, Вальдоксан (агомелатин), терапевтическая эффективность, переносимость.
Высокая распространенность депрессивных состояний, трудности их терапевтической коррекции, значимое влияние, которое они оказывают на социальную адаптацию, качество жизни пациентов, обусловливают постоянный интерес к поискам патогенетических механизмов возникновения и развития депрессий, а также оптимизации терапевтического подхода к этому контингенту больных.
В настоящее время существует несколько основных гипотез, на основании которых предпринимаются попытки объяснить патогенез депрессивных нарушений.
Одной из самых ранних гипотез, сформулированных в середине прошлого столетия, является моноаминовая, согласно которой в основе развития депрессии лежит дефицит моноаминов (норадреналина, серотонина) в ключевых областях головного мозга.
Однако депрессию невозможно объяснить только дисфункцией одного из моноаминов [1]. Так, имеющая место генная гипотеза постулирует, что депрессия возникает не столько из-за дефицита моноаминов, сколько из-за изменений в работе генов. Рецепторная гипотеза предполагает, что депрессия развивается не столько из-за уменьшения концентрации нейромедиаторных моноаминов в тканях мозга, сколько из-за нарушения функций рецепторных структур. Продолжаются исследования, направленные на изучение патофизиологических механизмов депрессии и разработку новых препаратов, действующих на гипофизарно-гипоталамо-надпочечниковую систему, нейропептидные рецепторы или промотирующих продукцию факторов роста и/или клеточной пролиферации в гиппокампе. Можно полагать, что все перечисленные механизмы являются звеньями патогенетического процесса, лежащего в основе развития депрессивных нарушений.
Еще одной концепцией развития депрессивных расстройств является хронобиологическая, основывающаяся на том, что депрессивные состояния нередко сопровождаются десинхронизацией биологических ритмов. Исходя из этого возникло предположение реализации антидепрессивного эффекта путем нормализации циркадианных ритмов [2, 3]. Водителем ритма для поддержания циркадианных циклических изменений в организме человека является супрахиазматическое ядро, расположенное в переднем гипоталамусе. Ключевую роль в синхронизации циркадианных ритмов, включая цикл «сон-бодрствование», выполняет хронобиотический гормон мелатонин, который синтезируется в эпифизе [4]. Синтез гормона мелатонина регулируется супрахиазматическим ядром, выработка его приходится на ночную фазу суточного цикла. Мелатонин поступает из эпифиза в супрахиазматическое ядро, где связывается с МТ1— и МТ2-рецепторами и осуществляет регуляцию циркадианных ритмов. Антидепрессивные свойства мелатонина не получили подтверждения в клинических исследованиях, однако послужили основой для создания препаратов, использующих свойства мелатонина.
В России Вальдоксан используется с 2008 г. К настоящему времени проведен ряд зарубежных и отечественных исследований, в том числе плацебо-контролируемых, а также исследования сравнительного характера 10.
Имеются данные о выраженной эффективности Вальдоксана при лечении умеренных и тяжелых депрессивных состояний непсихотического уровня у пациентов в стационарных и амбулаторных условиях [6, 7, 10-15].
Материал и методы исследования
Открытое несравнительное исследование поведено в отделе по изучению эндогенных психических расстройств и аффективных состояний НЦПЗ РАМН в течение 2010 г. Все пациенты дали добровольное письменное согласие на участие в исследовании.
Критерии включения.
Критерии исключения.
Высокий суицидальный риск (более 2 баллов по пункту 3 шкалы HDRS-21 и/или по клинической оценке исследователя); наличие психотических симптомов (т.е. наличие баллов по пунктам 18-21 шкалы HAMD-21); прием ингибиторов МАО в течение 2 недель до начала исследования; установленная ранее индивидуальная непереносимость Вальдоксана (агомелатина) или неудовлетворительный эффект применения Вальдоксана в анамнезе при назначении препарата в адекватной дозе (не менее 25 мг в сутки) и адекватной длительности (не менее 4 недель); наличие ряда психических расстройств (алкоголизм, наркомания) в анамнезе, тяжелых декомпенсированных заболеваний внутренних органов (почечная и/или печеночная недостаточность, злокачественные новообразования, метаболические заболевания, инсулинозависимый сахарный диабет, тиреотоксикоз); беременность или кормление грудью.
Таблица 1. Общие характеристики больных, участвующих в исследовании
| Пол | возраст (лет) ± SD | Тяжесть депрессии | Возраст начала заболевания | Длительность заболевания с манифестации (годы) | Длительность депрессии (мес) | Количество перенесенных аффективных фаз | ||
| умеренная | тяжелая | |||||||
| Муж. | 3 | 53±13,1 | 2 | 1 | 15,0±5,0 | 19,2±14,7 | 12,3±15,3 | 15,7±22,9 |
| Жен. | 23 | 34,9±12,1 | 15 | 8 | 25,1±13,8 | 10,1±9,6 | 6,87±8,6 | 4,0±3,2 |
| Все | 26 | 37,3±13,3 | 17 | 9 | 26,1±13,3 | 11,2±10,4 | 7,5±9,3 | 5,4±8,1 |
На период включения в исследование преобладающими в состоянии больных были жалобы на подавленное настроение. У 11 пациентов наряду с этим выявлялось выраженное чувство тревоги, нередко неопределенной, ни чем не мотивированной, сопровождающейся моторным беспокойством. В других 4 наблюдениях ведущим был тоскливый аффект, с локализацией щемящего чувства тоски преимущественно в загрудинной области. В состоянии 3 больных преобладали апато-адинамические, астенические проявления. У 8 пациентов наблюдалось различное сочетание аффективных компонентов, например тревожного аффекта с апато-адинамическими проявлениями, тревоги, перемежающейся с чувством тоски.
В структуре депрессивного состояния наиболее часто встречающимся симптомом было расстройство сна, на период начала исследования лишь 3 больных не предъявляли подобного рода жалоб. Трудности возникали преимущественно с процессом засыпания, этот период был особенно мучителен для больных. Также ухудшалось и качество сна, который был тревожный, с частыми пробуждениями и неприятным характером сновидений, сокращалась общая его продолжительность.
— CGI (Clinical Global Impression) c двумя подшкалами: CGI-S
До начала (Д0) и в ходе исследования для оценки безопасности применения и переносимости Вальдоксана наряду с клиническими параметрами анализировались показатели соматического состояния больного: масса тела, частота сердечных сокращений, уровень артериального давления, данные электрокардиографии, а также результаты общего и биохимического анализов крови.
Вальдоксан назначался однократно в день, в вечернее время, начиная с 25 мг; 16 больным уже в первые 2 нед при отсутствии явных признаков улучшения психического состояния и при условии хорошей переносимости препарата его доза повышалась до 50 мг, у остальных пациентов до конца исследования сохранялась терапевтически эффективная доза в 25 мг.
На каждого пациента исследователи заполняли карту, в которой регистрировались демографические показатели, диагноз, краткий медицинский анамнез, данные клинического состояния пациента, оцениваемого по шкалам, сопутствующие заболевания и их терапия, нежелательные явления, эффективность проводимого лечения.
Таблица 2. Основные статистические показатели для шкал депрессии HDRS-21 и СGI-S при терапии Вальдоксаном
| Дни визитов | HDRS-21 | CGI-S | ||||||
| Среднее значение ССБ (абс.) | СО* | R** | 95% ДИ*** | Среднее значение (абс.) | СО | R | 95% ДИ | |
| 0 | 24,42 | 4,47 | (22,70–26,14) | 4,35 | 0,49 | (4,16–4,53) | ||
| 3 | 21,42 | 5,99 | 12,28% | (19,12–23,73) | 3,92 | 0,69 | 9,73% | (3,66–4,19) |
| 5 | 19,00 | 6,34 | 22,20% | (16,56–21,44) | 3,69 | 0,68 | 15,04% | (3,43–3,95) |
| 7 | 17,38 | 6,23 | 28,82% | (14,99–19,78) | 3,50 | 0,91 | 19,47% | (3,15–3,85) |
| 14 | 12,08 | 7,19 | 50,55% | (9,31–14,84) | 3,00 | 0,89 | 30,97% | (2,66–3,34) |
| 21 | 9,00 | 6,20 | 63,15% | (6,62–11,38) | 2,54 | 0,90 | 41,59% | (2,19–2,89) |
| 28 | 7,96 | 5,78 | 67,40% | (5,74–10,18) | 2,35 | 1,13 | 46,02% | (1,91–2,78) |
| 42 | 5,58 | 5,01 | 77,17% | (3,65–7,50) | 1,85 | 0,92 | 57,52% | (1,49–2,20) |
| 56 | 3,81 | 3,35 | 84,41% | (2,52–5,09) | 1,46 | 0,81 | 66,37% | (1,15–1,77) |
*СО – стандартное отклонение; **R – коэффициент редукции; ***ДИ – доверительный интервал.
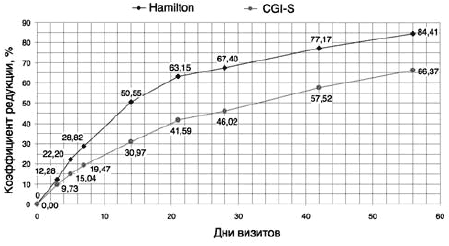
Рис. 1. Динамика коэффициента редукции ССБ по шкалам HDRS-21 и CGI-S при терапии Вальдоксаном.
Результаты исследования и их обсуждение
Все 26 больных, включенных в исследование, полностью завершили его, и по конечному результату у всех был отмечен терапевтический эффект. Проведена оценка тяжести депрессивного состояния на период завершения исследования и в динамике по группе в целом с использованием психометрических шкал CGI-S, CGI-I, шкалы депрессии HDRS-21 (табл. 2, рис. 1).
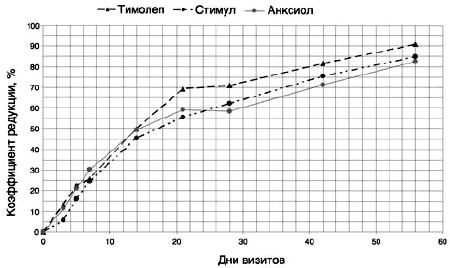
Рис. 2. Динамика коэффициента редукции ССБ, отражающего собственно тимолептический, стимулирующий, анксиолитический эффекты Вальдоксана
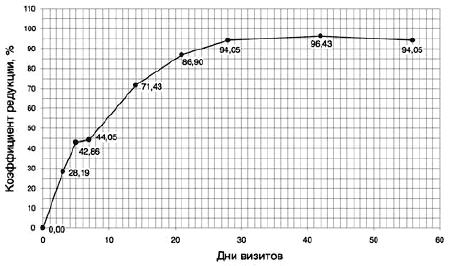
Рис. 3. Динамика коэффициента редукции ССБ признаков 4–6 (нарушения сна) по шкале депрессии HDRS-21.
Анализ показал 4 варианта индивидуальной динамики среднего балла по шкале HDRS-21 в исследуемой группе больных. Так, у подавляющего большинства из них (12 наблюдений) эффект развивался быстро, уже к 5-14-му дню терапии было характерно редуцирование среднего балла на 50% и выше, что свидетельствовало о «значительном» улучшении их состояния; в дальнейшем терапевтический эффект продолжал нарастать, но уже более медленными темпами. У 6 пациентов скорость наступления лечебного эффекта также была отчетливо выраженной, но 50% редукция среднего балла выявлялась на 14-21-й день терапии. В 4 наблюдениях кривая нарастания эффекта была пологой, а «значительный» терапевтический эффект развивался после 28 дня лечения. 2-я группа больных занимала как бы промежуточное положение между 1-й и 3-й подгруппами больных. Что касается 4 больных, то их состояние отличалось клинической нестабильностью, проявляющейся чередованием периодов улучшения/снижения глубины депрессии и ухудшения/нарастание глубины депрессии, в то же время в итоге к периоду завершения исследования клинический эффект оказался достаточно высоким и устойчивым. Мы не анализировали особенности разнообразия подобной динамики, для этого требуются больший объем исследуемого материала и иные методические подходы.
Как видно из табл. 2, по шкалам HDRS-21 и CGI-S статистические различия показателей в сопоставлении с Д0 выявляются уже к 5-му дню лечения. Полученные данные по терапевтическому эффекту Вальдоксана совпадают с результатами исследований, проведенных другими авторами.
Согласно существующим данным от 50 до 90% больных с депрессивной симптоматикой жалуются на нарушение сна. Расстройство сна, отражающее изменение суточного циркадианного ритма, биологических часов, регулирующих суточные колебания состояния организма, может проявляться изменением всех его стадий, а именно: увеличением длительности периода засыпания, неспокойным сном, неприятными по содержанию сновидениями, ранним пробуждением с невозможностью вновь заснуть. Установлено, что в сопоставлении с другими антидепрессантами Вальдоксан сокращает время засыпания и улучшает качество сна без сонливости в дневное время [10].
В настоящем исследовании был проведен анализ динамики среднего суммарного балла признаков 4-6 (ранняя бессонница, средняя бессонница, поздняя бессонница) шкалы депрессий HDRS-21 и коэффициента его редукции в ходе лечения Вальдоксаном (рис. 3).
За весь период исследования ни у одного из пациентов не наблюдалось появления новой продуктивной симптоматики.
Побочные эффекты
При оценке клинической эффективности препарата особое внимание уделялось анализу нежелательных явлений, которые возникали в ходе лечения и регистрировались независимо от их причинно-следственной связи с препаратом исследования. Оценка нежелательных (побочных) эффектов проводилась с использованием шкалы UKU с учетом их клинической характеристики, степени тяжести и длительности.
Нежелательные явления были выявлены всего лишь у одного больного. Они характеризовались появлением через неделю от начала лечения изжоги, неприятных ощущений в эпигастрии. По клиническим проявлениям они были отнесены к «автономным побочным эффектам» по шкале UKU. Следует отметить, что пациентка с перечисленными жалобами страдала хроническим гастритом. К терапии был добавлен фестал, мотилиум. Такое состояние продолжалось 4 дня, в дальнейшем описанная симптоматика не повторялась, лечение Вальдоксаном не прекращалось, доза препарата не менялась. Анализ таких параметров, как клинические и биохимические показатели крови, динамика массы тела, показатели электрокардиографии, не обнаружил клинически значимых отклонений в течение всего периода терапии.
Заключение
Проведенное 56-дневное исследование клинической эффективности и переносимости Вальдоксана (агомелатина) убедительно показало, что препарат обладает высокой терапевтической антидепрессивной активностью при лечении больных эндогенными депрессивными состояниями непсихотического уровня умеренной и тяжелой степени выраженности.
Особенностью препарата является раннее наступление терапевтического эффекта, который отчетливо проявлялся уже в первые 2 нед лечения, достигая значительной степени выраженности уже к 4-й неделе лечения и не уменьшался на дальнейших этапах его применения. К завершению исследования формирование ремиссии по шкале депрессии HDRS-21 наблюдалось у 76,9% из принявших участие в исследовании больных. Следует отметить, что полученные данные согласуются с результатами ранее проведенных работ.
Побочные эффекты применения Вальдоксана имеют невысокую частоту развития, минимальны по степени выраженности и в большинстве случаев транзиторны, не требуют отмены препарата, что, возможно, связано с отсутствием или слабо выраженной его способностью к связыванию с рядом рецепторов, в частности серотониновыми 5-HT1A-, 5-HT2-рецепторами, D1— и D2-допаминовыми рецепторами, α1-, α2-, ß-адренергическими, гистаминовыми H1-рецепторами, холинорецепторами, бензодиазепиновыми и опиоидными рецепторами. Следует отметить, что Вальдоксан может успешно применяться у больных, отягощенных соматическими заболеваниями, так как не вызывает их обострения.
Появление нового мелатонинергического антидепрессанта Вальдоксана (агомелатина), позволяет расширить возможности лечения пациентов с расстройствами депрессивного спектра и нарушениями сна, предотвратить рецидивы заболевания.
Сведения об авторах
Список использованной литературы