нормальная физиология практические навыки
Физа / Физа / Практика / Практические навыки
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
УЧРЕЖДЕНИЕ ОБРАЗОВАНИЯ «ГОМЕЛЬСКИЙГОСУДАРСТВЕННЫЙМЕДИЦИНСКИЙУНИВЕРСИТЕТ»
Кафедра нормальной физиологии
РУКОВОДСТВО К ПРАКТИЧЕСКИМ ЗАНЯТИЯМ
ПО НОРМАЛЬНОЙ ФИЗИОЛОГИИ
УДК 612 (076.5) ББК 28.073
Э. С.Питкевич, Э. М. Заика, В. А. Мельник, Н. И. Штаненко, С. Н. Мельник
заведующая кафедрой патологической физиологии Гомельского государственного медицинского университета, кандидат медицинских наук, доцент Т. С. Угольник
учеб.-метод. пособие / Э. С. Питкевич, [идр.]; подред. проф. Э. С. Питкевича. — Гомель: УО «Гомельский государственный медицинский уни-
верситет», 2008. — 128 с. ISBN 978-985-506-149-7
Настоящее учебно-методическое пособие включает лабораторные работы по всем разделам нормальной физиологии для студентов медицинских вузов. Материалы пособия изложены в соответствии с действующими программами по нормальной физиологии для студентов высших медицинских учебных заведений, утвержденных Министерством здравоохранения Республики Беларусь. В конце пособия располагаются базовые константы физиологических систем в Международной системе физических единиц (СИ).
Утверждено и рекомендовано к изданию Центральным учебным научнометодическим советом УО «Гомельский государственный медицинский университет» 11 апреля 2008 г., протокол № 5.
медицинский университет», 2008
Данное учебно-методическое пособие представляет собой материал для проведения лабораторных занятий по всем разделам нормальной физиологии для студентов медицинских вузов. Материалы пособия изложены в соответствии с действующими программами по нормальной физиологии для студентов высших медицинских учебных заведений, утвержденных Министерством здравоохранения Республики Беларусь.
Пособие состоит из введения, основной части, которая разделена на 36 лабораторный занятий и содержит материал по физиологии крови, сер- дечно-сосудистой, дыхательной и пищеварительной систем, физиологии выделения, обмена веществ и энергии, терморегуляции, возбудимых тканей, общей и частной физиологии ЦНС, физиологии желез внутренней секреции, анализаторов и высшей нервной деятельности. В конце пособия располагаются базовые константы физиологических систем в Международной системе физических единиц (СИ). В пособие включены материалы для самостоятельной работы студентов. В конце каждого раздела расположены контрольные вопросы к итоговому занятию.
Изучение методик лабораторных работ, включенных в пособие, позволит закрепить и облегчить более эффективное усвоение студентамимедиками полученных теоретических знаний и освоить некоторые важные клинико-диагностические методы исследования.
Ф И З И О Л О Г И Я К Р О В И
ЗАНЯТИЕ 1. ВВОДНОЕ ЗАНЯТИЕ ИНСТРУКТАЖ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ
Лабораторная работа 1.1. Методика забора крови из пальца
(Самостоятельная работа студентов под контролем преподавателя)
При заборе крови следует помнить о возможной ее инфицированности вирусом СПИДа, гепатита В и связанным с этим повышенным риском заражения, которому подвергаются лаборанты, проводящие серологические и клинические исследования. Поэтому при проведении анализа крови нужно руководствоваться правилами о профилактике СПИДа у медицинского персонала, занятого забором крови и ее исследованием.
Цель работы : освоить методику получения крови из пальца.
Для работы необходимы : одноразовый скарификатор, антисептическое средство, вата, предметные стекла. Объект исследования — человек.
1. Пациент должен сидеть напротив проводящего забор крови, рука (лучше левая) находится на столе.
2. Забор крови осуществляют из концевой фаланги 4-го пальца, что предотвращает распространение воспалительного процесса в случае его возникновения на кисть.
3. Кожа пальца дезинфицируется и обезжиривается антисептическим средством, остаткиантисептикаудаляютсясповерхностикожисухимватнымтампоном.
4. Открыть пакет с одноразовым скарификатором необходимо со стороны, противоположной колющей поверхности.
5. Прокол кожи делают в подушечке пальца в центральной точке, скарификатор погружают на всю глубину режущей поверхности.
6. Первую каплю крови снимают сухой ватой, тщательно вытирают палец (кожа должна быть сухой).
7. Следующаякаплякровидолжнаиметьвыпуклыйменискинерастекаться поповерхностикожи, изэтойипоследующейкапелькровьберетсядляанализа.
8. После забора крови место укола обрабатывается антисептическим средством.
Лабораторная работа 1.2.
Изучение свежего препарата крови под микроскопом
(Самостоятельная работа студентов с участием лаборанта)
Кровь состоит из жидкой части ― плазмы и взвешенных в ней клеток (форменных элементов): эритроцитов (красных кровяных телец), лейкоцитов (белых кровяных телец) и тромбоцитов (кровяных пластинок).
Цель работы : изучить особенности свежего препарата крови.
Для работы необходимы : капля свежей крови, микроскоп, предметные и покровные стекла, одноразовый скарификатор, вата, антисептическое средство. Объект исследования ― кровь человека.
Для рассмотрения свежего препарата крови под микроскопом каплю крови поместить на предметное стекло, накрыть покровным, выбрать поле для наблюдения с нетолстым слоем крови. Поле зрения занимают эритроциты, расположенные чаще всего в виде «монетных столбиков». Сделать рисунок, оформить вывод о закономерности расположения эритроцитов в свежем препарате крови.
ЗАНЯТИЕ 2. ФУНКЦИИ И СВОЙСТВА КРОВИ
Лабораторная работа 2.1. Определение гематокрита
(Самостоятельная работа студентов с участием лаборанта)
Гематокритом называют выраженное в процентах отношение объема форменных элементов к объему цельной крови.
Существует несколько методик определения гематокрита. Все они основаны на центрифугировании предотвращенной от свертывания крови, набранной в капилляр и измерении столбиков крови и осевших эритроцитов.
Цель работы: освоить методику определения гематокрита и определить его величину в исследуемой крови.
Для работы необходимы: гематокритный капилляр, центрифуга, одноразовый скарификатор, вата, антисептическое средство. Объект исследования ― кровь человека.
Выполнить прокол пальца по известной методике. Заполнить гематокритный капилляр не менее чем на 2/3 ее объема. Запломбировать концы трубочки пластилином и поместить в центрифугу (не менее двух капилляров во взаимно противоположных ячейках). Крышку центрифуги плотно закрутить. После центрифугирования измерить линейкой столбик набранной крови в трубочке. Измерить столбик эритроцитов в мм, вычислить процентное соотношение. За 100% принять длину столбика всей набранной крови, за Х ― длину столбика эритроцитов. Найденное значение Х% будет соответствовать показателю гематокрита крови. Для перевода гематокрита, выраженного в % в единицы системы СИ полученную величину умножить на 0,01.
В выводе сравнить полученный показатель гематокрита с нормой.
Лабораторная работа 2.2. Подсчет количества эритроцитов
(Самостоятельная работа студентов с участием лаборанта)
Цель работы: освоить методику и определить количество эритроцитов в исследуемой крови.
Для работы необходимы: микроскоп, счетная камера Горяева, меланжер для эритроцитов, 3% раствор хлорида натрия, покровные стекла, автоматическая пипетка, пробирки, одноразовый скарификатор, вата, антисептическое средство. Объект исследования ― кровь человека.
Перед началом работы необходимо рассмотреть счетную камеру под микроскопом, найти малые квадратики и большие квадраты сетки (рисунок 1). Камеру предварительно необходимо подготовить путем притирания покровного стекла к боковым выступающим граням камеры до появления цветных (ньютоновских) колец. В каплю свежей крови, полученной из пальца, погрузить кончик меланжера (с красной бусинкой в расширении) для эритроцитов и набрать кровь до метки 0,5, следя, чтобы в капилляр не попали пузырьки воздуха. Быстро, пока кровь не свернулась, перенести кончик меланжера в 3% раствор хлорида натрия и набрать его до метки 101, т.е. развести кровь в 200 раз. После этого взять заполненный меланжер (смеситель), зажать его концы 1 и 3 пальцами и в течение 1 мин встряхивать. После тщательного перемешивания крови, удалив предварительно 1–2 капли, нанести небольшую капельку на сетку камеры.
При необходимости такое же разведение может быть выполнено другим способом. Например, 0,02 мл крови смешать с 4 мл 3% NaCl в пробирке. Содержимое пробирки в этом случае тщательно перемешивается.
Рисунок 1 — Приборы для подсчета форменных элементов крови:
а ― счетная камера Горяева вид сверху, б ― вид сбоку;
в ― смесители для подсчета эритроцитов и г ― лейкоцитов, д ― сетка счетной камеры
Заполнив камеру, поместить ее под микроскоп и, если форменные элементы расположены равномерно (что является показателем хорошего перемешивания крови), приступить к подсчету. Считать эритроциты удобнее при большом увеличении.
Необходимо подсчитать число эритроцитов в 5 больших квадратах, расположенных в разных местах сетки, например, по диагонали. Во избежание двухкратного подсчета клеток, лежащих на границе между малыми квадратиками, руководствоваться правилом Егорова, согласно которому, относящимися к данному квадратику считаются эритроциты, лежащие как внутри квадратика, так и на его левой и верхней границе. Эритроциты, лежащие на правой и нижней границе для данного квадратика не учитываются.
Формула для вычисления количества эритроцитов в 1 мм 3 крови:
где: N ― искомое число эритроцитов;
А ― число эритроцитов в 80 маленьких квадратиках (или в 5 больших); 4000 ― множитель для получения содержания эритроцитов в одном мм 3 крови; 200 ― степень разведения эритроцитов.
Для перевода полученного количества эритроцитов в единицы СИ, подсчитанное количество эритроцитов умножить на 10 6 и выразить в N х 10 12 /л. Зарисовать фрагмент сетки камеры Горяева с маленькими и большими квадратами.
В выводе сравнить количество подсчитанных эритроцитов с нормой.
ЗАНЯТИЕ 3. ФИЗИОЛОГИЯ ЭРИТРОЦИТОВ
Лабораторная работа 3.1. Определение количества гемоглобина в крови по способу Сали
(Самостоятельная работа студентов с участием лаборанта)
Определение содержания гемоглобина в крови производится колориметрическими способами, один из которых (гематиновый метод Сали) основан на образовании устойчивого раствора коричневого цвета при взаимодействии гемоглобина с соляной кислотой. Принцип колориметрического способа заключается в том, что если исследуемый раствор путем разбавления довести до окраски, одинаковой со стандартным раствором, то концентрация растворенных веществ в обоих растворах будет одинакова. В стандартном растворе гемоглобина содержится 167 г/л.
Цель работы: освоить методику определения гемоглобина и найти содержание гемоглобина в исследуемой крови.
Для работы необходимы: гемометр Сали, капилляр с меткой 0,02 мл, 0,1 нормальный раствор соляной кислоты, дистиллированная вода, свежая кровь, пипетка, стеклянная палочка, вата, антисептическое средство, одноразовый скарификатор. Объект исследования ― кровь человека.
В среднюю пробирку гемометра налить 0,1 нормальный раствор соляной кислоты до нижней кольцевой метки. Из пальца обычным способом набрать в капилляр (рисунок 2) кровь без пузырьков до метки.
Рисунок 2 ― Гемометр Сали и капилляр. (Пояснение в тексте)
Излишек крови можно удалить из капилляра прикладыванием ваты или фильтровальной бумаги к кончику капилляра. Выдуть кровь на дно пробирки из капилляра так, чтобы верхний слой кислоты остался неокрашенным. Не вынимая капилляр, промыть его раствором соляной кислоты из верхнего слоя пробирки гемометра. После этого содержимое пробирки перемешать стеклянной палочкой и поставить в гемометр на 5–10 мин. Это время необходимо для полного превращения гемоглобина в солянокислый гематин.
Затем к содержимому пробирки прибавить по каплям дистиллированную воду, каждый раз перемешивая раствор стеклянной палочкой до тех пор, пока цвет полученного раствора не станет одинаковым с цветом стандартного раствора боковых ампул гемометра. Цифра, стоящая на уровне нижней границы мениска полученного раствора отражает содержание гемоглобина в исследуемой крови в грамм-процентах (г%).
Перевод полученных данных в единицы системы СИ (в г/л) производят путем умножения измеренного количества гемоглобина в г% на 10. Зарисовать гемометр и капилляр. В выводе сравнить с нормой полученное содержание гемоглобина в исследуемой крови.
Лабораторная работа 3.2. Определение гемоглобина крови гемоглобинцианидным (фотоэлектроколориметрическим) методом
(Самостоятельная работа студентов с участием лаборанта)
Цель работы: освоить методику определения гемоглобина крови гемоглобинционидным методом и определить содержание гемоглобина в исследуемой крови.
Для работы необходимы: фотоколориметр, пипетки на 0,02 мл и 5,0 мл, пробирки, кюветы толщиной 1 см, приготовленный трансформирующий раствор из набора, вата, антисептическое средство, одноразовый скарификатор. Объект исследования ― кровь человека.
Приготовить опытную пробу. Для этого к 5 мл приготовленного трансформирующего раствора добавить 0,02 мл полученной из пальца цельной крови. Разведение крови в этом случае составит 251. Полученный раствор тщательно перемешать, выдержать 5–10 минут, а затем перенести в кювету фотоэлектроколориметра.
Приготовить кювету с трансформирующим раствором. Для этого отмерить 5 мл трансформирующего раствора и перенести его в аналогичную кювету (как для разбавленной крови).
Совместно с лаборантом произвести измерение согласно инструкции прибора. Измерения проводятся не менее 3 раз и затем вычислить среднюю арифметическую.
Расчет содержания гемоглобина в исследуемой крови произвести по формуле:
где: Е оп ― экстинкция опытной пробы; Е ст ― экстинкция стандартного раствора (определяется однократно для одного
набора из 200 проб); С ― концентрация гемоглобинцианида (59,8 мг/%);
К ― степень разведения крови (в 251 раз).
Ввыводесодержаниегемоглобинависследуемойкровисравнитьснормой. Перевести количество гемоглобина вединицы СИ. Для этогополученные
поформулезначенияумножитьна10 ивыразитьрезультаты вг/л.
Лабораторная работа 3.3. Определение цветового показателя крови
Цветовой показатель (ЦП) отражает насыщенность эритроцитов гемоглобином.
Цель работы: освоить методику и рассчитать ЦП крови.
Для работы необходимы: данные количества эритроцитов и содержания гемоглобина в крови, полученные при выполнении лабораторной работы 2 занятия 2 и лабораторной работы 1 занятия 3.
У испытуемого определяют количество эритроцитов и гемоглобина в крови. Расчет цветового показателя производят по формуле:
где: А ― число эритроцитов в 1 мкл (первые три цифры).
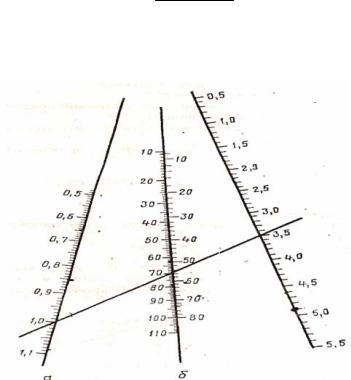
ЦП можно определить по номограмме (рисунок 3).
Рисунок 3 — Номограмма для определения величины цветового показателя:
а ― шкала величин цветового показателя, б ― шкала процентного содержания гемоглобина по Сали, в ― число эритроцитов в одном мкл.
Полученную величину цветового показателя сравнить с нормой.
ЗАНЯТИЕ4. ФИЗИОЛОГИЯЛЕЙКОЦИТОВ. СВЕРТЫВАНИЕКРОВИ
Лабораторная работа 4.1. Подсчет количества лейкоцитов
(Самостоятельная работа студентов с участием лаборанта)
Цель работы: освоить методику и определить количество лейкоцитов в исследуемой крови.
Для работы необходимы: микроскоп, счетная камера Горяева, меланжер для подсчета лейкоцитов, 5% раствор уксусной кислоты, подкрашенный метиленовым синим, покровные стекла, автоматическая пипетка,
Физиология: практические навыки
Материальное оснащение, описание и способы выражения практических результатов при измерениях физиологических показателей: динамометрии, определении количества гемоглобина, подсчете числа эритроцитов и лейкоцитов, вычислении цветового показателя.
| Рубрика | Медицина |
| Вид | методичка |
| Язык | русский |
| Дата добавления | 17.03.2014 |
| Размер файла | 49,7 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Материальное оснащение: динамометры кистевой ДРП-120 и становой ДС-200.
Испытуемый в положении стоя отводит вытянутую руку с динамометром в сторону под прямым углом к туловищу. Вторая свободная рука опущена и расслаблена. По сигналу экспериментатора испытуемый дважды выполняет максимальное усилие на динамометре. Силу мышц оценивают по лучшему результату. Определяется сила мышц правой, а затем левой руки (в кг).
К специальной платформе присоединяется становой динамометр. Испытуемый становится на платформу, берет рукоятки динамометра и производит максимальное разгибание туловища. По показаниям динамометра оценивают силу мышц-разгибателей спины.
Выражение практического результата
Силу мышц кисти и становую силу выражают в кг.
2. Определение количества гемоглобина
Материальное оснащение: гемометр Сали, пипетки, стеклянная палочка, пипетка с меткой 0,02 мл, груша, 0,1 н раствор HСl, вода дистиллированная, вата, донорская кровь
В среднюю пробирку гемометра Сали наливают 0,1 н раствор хлористоводородной кислоты до нижней метки. Пипеткой берут 20 мм 3 (0,02 мл) донорской крови и, обтерев кончик ее ватой, тотчас выдувают кровь на дно пробирки так, чтобы верхний слой кислоты оставался неокрашенным. Не вынимая пипетку, споласкивают ее кислотой. После этого содержимое пробирки перемешивают, ударяя пальцем по дну пробирки, и ставят в штатив на 5-10 мин. Это время необходимо для полного превращения гемоглобина в солянокислый гематин. Затем к содержимому пробирки добавляют по каплям дистиллированную воду до тех пор, пока цвет полученного раствора не будет совершенно одинаков с цветом стандарта (добавляя воду, раствор перемешивают стеклянной палочкой).
Цифра, стоящая на уровне полученного раствора, показывает содержание гемоглобина в испытуемой крови.
Выражение практического результата
Содержание гемоглобина выражают в г/л. В норме содержание гемоглобина составляет для мужчин 133-158 г/л, для женщин 121-138 г/л.
Определение количества гемоглобина на фотоэлектроколориметре (по методу Драбкина, Кросби и Кюннена
Материальное оснащение: фотоэлектроколориметр, кюветы на 10 мм, пипетка от гемометра Сали с меткой 0,02 мл, груша, реактив Драбкина (бикарбонат натрия, углекислый натрий, цианид калия, красная кровяная соль), пипетка на 5,0 мл, стеклянная палочка, донорская кровь, дистиллированная вода.
В пробирку наливают 5,0 мл реактива Драбкина. Пипеткой от гемометра Сали набирают 0,02 мл крови и переносят в реактив. Раствор тщательно перемешивают стеклянной палочкой. Через 10 минут (это время необходимо для образования цианметгемоглобина, обладающего устойчивой окраской) его помещают в кювету шириной 10 мм и фотоколориметрируют при длине волны 540 10 нм против дистиллированной воды.
Выражение практического результата
3. Подсчет числа эритроцитов
Материальное оснащение: дозатор (или унипипетка) на 0,02 мл, пробирка, камера Горяева, микроскоп, стеклянная палочка или пастеровская пипетка, изотонический раствор NaCl, донорская кровь, груша, спирт, вата, игла-скарификатор одноразового пользования.
В пробирку наливают 4 мл изотонического раствора NaCl. Пипеткой от гемометра Сали набирают 0,02 мл крови и переносят в раствор NaCl. Тщательно перемешивают и небольшую каплю раствора (стеклянной палочкой или пастеровской пипеткой) наносят на среднюю пластинку камеры Горяева. По принципу капиллярности она устремляется под покровное стекло. Предварительно к камере должно быть притерто покровное стекло. Чтобы его притереть, нужно ватой, смоченной в спирте, обезжирить боковые пластинки камеры и само стекло. Критерием полного притирания является появление на боковых пластинках камеры цветных колец Ньютона. Считать эритроциты удобнее при большом увеличении (окуляр 7, объектив 40). Чтобы получить точные результаты, необходимо подсчитать число эритроцитов в 5 больших квадратах, расположенных в разных местах сетки, например по диагонали. Подсчитав число эритроцитов (А) в 5 больших квадратах (что составляет 80 маленьких), подставляют значение А в формулу:
Выражение практического результата
Количественное содержание эритроцитов выражают в литре крови. В норме содержание эритроцитов у мужчин 4,5-510 12 в литре; у женщин 3,9-4,510 12 в литре.
4. Вычисление цветового показателя
Практически цветовой показатель (ЦП) вычисляют делением показателей концентрации гемоглобина, выраженной в г/л, на число первых трех цифр количества эритроцитов в 1 мкл крови с последующим умножением полученного частного на 3.
Выражение практического результата
Результат выражают в относительных единицах. В норме (нормохромазия) цветовой показатель равен 0,9-1,1.
5. Подсчет числа лейкоцитов
Материальное оснащение: пипетка с меткой 0,02 мл от гемометра Сали, пробирка, камера Горяева, микроскоп, груша, 3% раствор уксусной кислоты, подкрашенный метиленовым синим, донорская кровь, спирт, вата.
В пробирку наливают 0,4 мл 3% раствора уксусной кислоты, подкрашенной метиленовой синью. Набирают пипеткой от гемометра Сали 0,02 мл крови и переносят в раствор уксусной кислоты. Тщательно перемешивают и небольшую каплю раствора (стеклянной палочкой или пастеровской пипеткой) наносят на среднюю пластинку камеры Горяева. По принципу капиллярности она устремляется под покровное стекло. Предварительно к камере должно быть притерто покровное стекло. Чтобы его притереть, нужно ватой, смоченной в спирте, обезжирить боковые пластинки камеры и само стекло. Критерием полного притирания является появление на боковых пластинках камеры цветных колец Ньютона. Считать лейкоциты удобнее при малом увеличении (окуляр 15, объектив 20).
Чтобы получить точные результаты, необходимо подсчитать число лейкоцитов в 25 больших квадратах сетки Горяева, что составляет 400 маленьких квадратов. Подсчитав число лейкоцитов (В) в 25 больших квадратах (это 400 маленьких), подставляют значение В в формулу:
Объем маленького квадрата равен:
Выражение практического результата
Количественное содержание лейкоцитов выражают в литре крови. В норме содержание лейкоцитов 4-810 9 в литре.
физиологический показатель измерение практический
6. Определение групповой принадлежности крови (система АВ0)
Материальное оснащение: гемагглютинирующие сыворотки групп 0 (I), А (II), В (III) двух различных серий, сыворотка группы АВ0 (IV), изотонический раствор NaCl, пипетки, предметные стекла или стеклянные палочки, планшет для определения групп крови, донорская кровь, игла-скарификатор одноразового пользования, спирт, вата.
Техника определения групп крови при помощи стандартных гемагглютинирующих сывороток
Другой стеклянной палочкой (или другим краем предметного стекла) перемешивают каплю крови с сывороткой группы 0 (I) до тех пор, пока смесь не окрасится в равномерно розовый цвет. Следующей стеклянной палочкой (другим углом стекла) перемешивают следующую каплю крови с сывороткой группы А (II) и также поступают с сывороткой группы и В (III). Так же смешивают кровь с сыворотками во втором ряду.
После размешивания капель планшет покачивают, затем на 1 минуту оставляют в покое и снова периодически покачивают. Наблюдение за ходом реакции производят при легком покачивании планшета в течение 5 минут. Агглютинация наступает обычно в течение первых 19-30 секунд, однако наблюдение производят не менее 5 минут ввиду возможности позднего наступления агглютинации в случае слабой агглютинабельности эритроцитов (А2 или А2В).
Результат реакции в каждой капле может быть положительным (+) или отрицательным (-).
Группу крови устанавливают в зависимости от наличия или отсутствия реакции изогемагглютинации. Оценку результата см. на рисунке 1.
Результаты реакций в каплях с сыворотками могут дать четыре различных комбинации положительных и отрицательных реакций.
1. Если сыворотки всех трех групп дали отрицательную реакцию, т.е. все смеси остались равномерно окрашенными в розовый цвет без признаков агглютинации, то испытуемая кровь не содержит агглютиногенов и, следовательно, принадлежит к группе 0 (I).
Выражение практического результата:
7. Определение резус-принадлежности крови
Материальное оснащение: пробирка, пипетки Пастера, стандартный реагент антирезус Rh0 (D), изотонический раствор NaCl, цельная донорская кровь, игла, спирт, вата.
На дно пробирки вносят 1 каплю стандартного реагента антирезус Rh0 (D) и 1 каплю исследуемой крови (или эритроцитов). Содержимое пробирки перемешивают встряхиванием и затем медленно поворачивают, наклоняя пробирку почти до горизонтали таким образом, чтобы содержимое растекалось по ее стенкам. Такое размазывание крови по стенкам пробирки делает реакцию более выраженной. Как правило, агглютинация наступает в течение 1-й минуты, но для образования устойчивого комплекса антиген+антитело и четко выраженной агглютинации, а также ввиду возможности замедленной реакции при слабо выраженной агглютинабельности эритроцитов контакт эритроцитов с реагентом при повертывании пробирки следует проводить не менее 3 мин. Затем для исключения неспецифической агрегации эритроцитов в пробирку добавить 2-3 мл изотонического раствора NaCl и перемешать, не взбалтывая, путем 2-3-кратного перевертывания пробирки. Если агрегация эритроцитов была неспецифической, то после добавления изотонического раствора она исчезает. Наличие агглютинации оценивается визуально, в неясных случаях проводят микрокопирование.
Наличие агглютинации в виде крупных хлопьев из эритроцитов на фоне просветленной жидкости указывает на резус-положительную принадлежность исследуемой крови (Rh + ), содержащей антиген Rh0 (D).
Результат учитывается как истинный после проверки контрольных образцов, т.е. при положительном результате со стандартными резус-положительными эритроцитами той же группы или группы 0 (I) по системе АВ0 и отсутствии агглютинации со стандартными резус-отрицательными эритроцитами, одногруппными с исследуемой кровью по системе АВ0.
Выражение практического результата
Резус-принадлежность крови выражается буквенным обозначением и расшифровкой при обязательном указании группы крови по системе АВ0. Например: кровь испытуемого (донора) (Ф.И.О.) группы 0 (I) резус Rh + (положительная).
8. Определение частоты пульса
Материальное оснащение: секундомер или часы с секундной стрелкой.
У здорового человека сокращения сердца и пульсовые волны следуют друг за другом через равные промежутки времени, т.е. пульс ритмичный (pulsus regularis). При ритмичном пульсе счет пульса обычно проводят за 30, 15 или 10 с и найденное число умножают соответственно на 2, 4 или 6, определяя число пульсовых ударов за 1 мин.
В нормальных условиях частота пульса соответствует частоте сердечных сокращений и равна 60-80 в минуту. При учащении сердечных сокращений выше 90 (синусовой тахикардии) увеличивается число пульсовых волн в минуту, регистрируют частый пульс (pulsus freguens), при замедлении сердечного ритма ниже 60 (синусовой брадикардии) регистрируют редкий пульс (pulsus rarus).
Частота пульса определяется не только состоянием сердечной мышцы, нервного аппарата сердца, способности к выработке импульсов самим синусно-предсердным узлом, но и экстракардиальными влияниями. Иногда редкий пульс, т.е. менее 60 ударов в минуту, встречается у совершенно здоровых людей ваготоников и хорошо тренированных спортсменов.
Волнение, эмоциональное напряжение (стресс), физическая нагрузка приводят к учащению пульса. Частота пульса зависит также и от температуры тела. Следует учитывать, что каждому повышению температуры тела на 1 о С соответствует учащение пульса на 8-10 ударов.
Зная пульс, можно рассчитать длительность сердечного цикла по следующей пропорции: например, при частоте пульса 70 в мин.:
70 сокращений за 60 с
Длительность сердечного цикла колеблется в пределах 0,75-1,0 с.
Выражение практического результата
Подсчитав частоту пульса лучевой артерии у себя или у коллеги, записывают, например:
Пульс испытуемого (Ф.И.О.) в покое ритмичный (pulsus regularis), 75 уд/мин, что соответствует норме (60-80 уд/мин).
Или: пульс испытуемого (Ф.И.О.) ритмичный, частый (pulsus freguens), 92 уд/мин, что соответствует тахикардии (например, в условиях волнения, эмоционального напряжения).
9. Определение артериального давления (АД) методом Короткова
Материальное оснащение: сфигмоманометр, фонендоскоп.
1) оптимальное: систолическое АД
© 2000 — 2021, ООО «Олбест» Все права защищены