Эссенциальный тромбоцитоз что это такое и как лечить
Эссенциальный тромбоцитоз что это такое и как лечить
Целями лечения при эссенциальной тромбоцитемии являются:
1) нормализация числа тромбоцитов;
2) профилактика тромботических и геморрагических осложнений.
Нормализация количества тромбоцитов при эссенциальной тромбоцитемии
Для циторедукции в качестве терапии первой линии используются:
1) гидроксимочевина,
2) анагрелид;
3) а-интерферон.
Циторедуктивная терапия обязательна при количестве тромбоцитов более 1500 • 10 9 /л, при меньшем тромбоцитозе лечение назначают по дифференцированным показаниям. При высоком тромбоцитозе, тромбофилических и геморрагических осложнениях гидроксимочевину назначают по 2-4 г/сут за 2 приема с постепенным уменьшением до 1 г и до 0,5 г при достижении ремиссии.
При умеренном лейкоцитозе доза составляет 15 мг/(кг•сут) с дальнейшим переходом на поддерживающую терапию.
Анагрелид используется при необходимости быстрого снижения количества тромбоцитов, особенно у лиц молодого возраста, при развитии сосудистых осложнений и подготовке к операции. Начальная доза препарата составляет 0,5 мг каждые 12 часов в течение 7 дней, в дальнейшем доза увеличивается на 0,5 мг/сут еженедельно до наступления эффекта.
Максимальная рекомендуемая суточная доза — 3,5-4 мг. Поддерживающая терапия проводится в дозе 2-2,5 мг/сут. При лечении необходим тщательный контроль состояния сердечно-сосудистой системы (ЭКГ, ЭхоКГ).
Интерферон-альфа эффективно подавляет продукцию тромбоцитов и практически не обладает лейкозогенным действием. Схема лечения аналогична другим хроническим миелопролиферативным заболеваниям: 1 млн ME подкожно в первый день, 2 млн ME во второй день и по 3 млн ME ежедневно с третьего дня.
Оценка ответа производится через 6 месяцев. При полной клинико-гематологической ремиссии (достигается у 90% больных) отмечается нормализация размеров селезенки, количество тромбоцитов меньше 400•10 9 /л. При достижении полного ответа лечение в поддерживающей дозе (3 млн ME 3 раза в неделю) проводится в течение двух лет.
При развитии частичной ремиссии размеры селезенки уменьшаются на 50% от исходных, количество тромбоцитов не превышает 600•10 9 /л. В этом случае к лечению добавляют гидроксимочевину в дозе 500-1500 мг/сут и продолжают лечение еще в течение 6 месяцев. В дальнейшем в зависимости от результатов лечения переходят на поддерживающую терапию или используют другие препараты.
Лечение и профилактика сосудистых осложнений при эссенциальной тромбоцитемии
При микрососудистых тромбофилических осложнениях применяется ацетилсалициловая кислота, при отсутствии эффекта дополнительно назначаются низкомолекулярный гепарин и трансфузии свежезамороженной плазмы (400 мл 2 раза в неделю). Для быстрого снижения уровня тромбоцитов используют тромбоцитаферез.
Для лечения геморрагического синдрома в ряде случаев требуются трансфузии концентрата тромбоцитов, поскольку тромбоциты больных эссенциальной тромбоцитемией качественно неполноценны.
Для профилактики микроциркуляторных тромбофилических осложнений до достижения гематологической ремиссии и у больных с ремиссией — по дополнительным показаниям используется ацетилсалициловая кислота в дозе 40-300 мг/сут.
Прогноз эссенциальной тромбоцитемии
Эссенциальная тромбоцитемия — индолентное заболевание, которое характеризуется длительным бессимптомным течением с редкими тромбоэмболическими или геморрагическими осложнениями. Вероятность летального исхода, обусловленного тромбозами, трансформацией в острый миелоидный лейкоз или миелодиспластические синдромы (в связи с предшествующей цитотоксической терапией), менее 5%.
Медиана выживаемости превышает 10-15 лет. В связи с тем что в большинстве случаев заболевание возникает в среднем и пожилом возрасте, продолжительность жизни обычно не отличается от популяционной.
Необходимо помнить, что селезенка является местом секвестрации тромбоцитов, поэтому спленэктомия часто приводит к резкому нарастанию тромбоцитоза и ухудшению прогноза.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Эссенциальный Тромбоцитоз
(эссенциальный тромбоцитоз; первичная тромбоцитемия)
, MD, James P. Wilmot Cancer Institute, University of Rochester Medical Center
Этиология эссенциальной тромбоцитемии
Патофизиология эссенциального тромбоцитоза
Тромбоцитемия может привести к:
Окклюзии мелких сосудов (обычно обратимы)
Тромбозу крупных сосудов
Остается неясным, повышен ли риск тромбоза крупных сосудов, вызывающего тромбоз глубоких вен или легочную эмболию у пациентов с эссенциальной тромбоцитемией, частично из-за того, что тромбоциты в первую очередь участвуют в артериальном тромбозе, и нет корреляции между количеством тромбоцитов и тромбозом крупных сосудов.
Симптомы и признаки эссенциальной тромбоцитемии
К частым симптомам относятся:
Кровоподтеки и кровоизлияния
Парестезии кистей рук и стоп
Тромбоз может вызывать симптомы в пораженном участке (например, неврологический дефицит при инсульте или транзиторных ишемических атаках).
Кровотечения, как правило, небольшие, редко спонтанные и проявляются эпистаксисом, желудочно-кишечными кровотечениями или склонностью к образованию гематом. Однако в небольшом проценте случаев тяжелого тромбоцитоза может возникнуть тяжелое кровотечение.
Может появиться эритромелалгия (жгучие боли в руках и ногах, сопровождающиеся приливом жара, эритемой и, иногда, дигитальной ишемией). Селезенку можно пропальпировать, но значительная спленомегалия не характерна для данной патологии и может предполагать наличие другого миелопролиферативного новообразования.
Диагностика эссенциального тромбоцитоза
Общий анализ крови (ОАК) и мазок периферической крови
Исключение причин вторичного тромбоцитоза
JAK2 мутации диагностируют с помощью полимеразной цепной реакции и, если результат отрицательный, исследуют на мутации CALR или MPL
Возможно исследование костного мозга
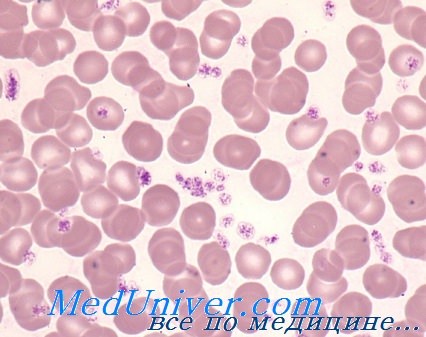
Количество тромбоцитов> 450 000/мкл ( > 450 000 × 10 9 /л), но может составлять > 1 000 000/мкл ( > 1 000 000 × 10 9 /л). Уровень тромбоцитов может снижаться во время беременности. В мазке периферической крови могут обнаруживаться гигантские тромбоциты и фрагменты мегакариоцитов.
При подозрении на идиопатическую тромбоцитемию следует провести общий анализ крови, мазок периферической крови, исследования железа и генетические исследования, включая количественный анализ на JAK2 V617F и анализ на BCR-ABL. Это следует сделать для исключения хронического миелолейкоза Хронический миелолейкоз (ХМЛ) Хронический миелолейкоз (ХМЛ) развивается в результате злокачественной трансформации и клональной пролиферации плюрипотентных стволовых клеток, приводящей к гиперпродукции зрелых и незрелых. Прочитайте дополнительные сведения (ХМЛ, который может проявляться только тромбоцитозом). Если анализы на JAK2 и BCR-ABL отрицательные, должны быть проведены анализы на мутации CALR и MPL. Диагноз эссенциальной тромбоцитемии предполагают на основании нормального гематокрита, количества лейкоцитов, среднего объема эритроцитов (MCV) и исследования уровня железа, а также отсутствия транслокации BCR-ABL
Согласно рекомендациям Всемирной организации здравоохранения, для диагностики эссенциальной тромбоцитемии необходимо, чтобы биопсия костного мозга показывала повышенное количество увеличенных, зрелых мегакариоцитов, но этот критерий никогда не подлежал перспективной валидации, и исследование костного мозга не может дифференцировать эссенциальную тромбоцитопению от истинной полицитемии. Тем не менее, биопсия костного мозга выполняется для определения выраженности фиброза.
Прогноз при эссенциальном тромбоцитозе
Продолжительность жизни близка к нормальной. Хотя заболевание часто сопровождается симптомами, его течение обычно доброкачественное. Серьезные осложнения, обусловленные тромбозом артерий, встречаются редко, но могут представлять угрозу для жизни. Трансформация в лейкоз отмечается у 2% пациентов, но её вероятность может возрастать после применения цитотоксических препаратов, в том числе гидроксимочевины. У некоторых пациентов развивается вторичный миелофиброз, который чаще наблюдается у мужчин с мутацией JAK2V617F или CALR 1 типа.
Лечение эссенциального тромбоцитоза
Препараты, снижающие уровень тромбоцитов (например, гидроксимочевина (в РФ не зарегистрирована), анагрелид)
В редких случаях, цитотоксическое средство
В редких случаях, интерферон
Редко, пересадка гемопоэтических стволовых клеток
При незначительно выраженных вазомоторных симптомах (таких как головная боль, легкая степень ишемии пальцев, эритромелалгия) с целью снижения риска тромбоза у пациентов из группы низкого риска обычно достаточно применения аспирина в дозе 81 мг/день перорально, но при необходимости могут применяться большие дозы. Для контроля тяжелой мигрени может потребоваться снижение количества тромбоцитов. Польза аспирина в период беременности не доказана, его прием может спровоцировать кровотечение у пациенток с эссенциальной тромбоцитемией и мутацией CALR.
Использование аминокапроновой или транексамовой кислот является эффективным в борьбе с кровотечением, вызванным приобретенным синдромом Виллебранда во время проведения незначительных вмешательств, таких как стоматологические процедуры. Проведение более серьезных процедур требует оптимизации количества тромбоцитов.
Снижение количества тромбоцитов
Поскольку прогноз обычно благоприятен и нет корреляции между степенью тромбоцитоза и тромбозом, потенциально токсичных препаратов, снижающих уровень тромбоцитов, следует избегать, чтобы нормализовать количество тромбоцитов у пациентов с отсутствием клинических симптомов. К общепризнанным показаниям для снижения уровня тромбоцитов относятся:
Факторы сердечно-сосудистого риска
Транзиторными ишемическими атаками
Необходимость хирургического вмешательства у пациентов с тяжелым тромбоцитозом и низкой активностью кофактора ристоцетина
Иногда тяжелая мигрень
Тем не менее нет никаких данных, которые подтверждают, что использование цитотоксической терапии для уменьшения количества тромбоцитов снижает риск образования тромбов или улучшает выживаемость. JAK2-положительные и/или пациенты возрастом старше 65 лет подвергаются наибольшему риску развития тромбоэмболических осложнений.
К препаратам, которые снижают уровень тромбоцитов, относятся анагрелид, интерферон альфа-2b и гидроксимочевина. В целом гидроксимочевина считается препаратом выбора для кратковременного использования. Поскольку гидроксимочевина (в РФ не зарегистрирована) и анагрелид проходят через гематоплацентарный барьер, они не используются во время беременности. При необходимости беременным может назначаться интерферон альфа-2a. При условии неэффективности средств для мигрени, самой безопасной терапевтической стратегией для лечения мигрени является применение интерферона. Анагрелид необходимо с осторожностью использовать у пожилых пациентов из-за его влияния на сердечно-сосудистую систему (например, сердцебиение, аритмии) и почки (например, задержка жидкости).
Гидроксимочевину следует назначать только тем специалистам, которые знакомы с особенностями ее использования и мониторинга. Его назначают в начальной дозе от 500 до 1000 мг перорально 1 раз/день. Пациентам еженедельно выполняют общий анализ крови. Если количество лейкоцитов снижается 4000/мкл ( 4 × 10 9 /л), прием гидроксимочевины останавливают и повторно вводят в половинной дозе до нормализации количества лейкоцитов. При достижении стабильного состояния, интервал между проведением ОАК удлиняется до 2 недель, а затем до 4 недель. Целью проводимого лечения является облегчение симптомов, а не нормализация количества тромбоцитов. Слишком резкая отмена приема гидроксимочевины может привести к быстрому скачку количества тромбоцитов.
Действие руксолитиниба, препарата, который используется при истинной полицитемии и первичном миелофиброзе, было изучено на пациентах с эссенциальной тромбоцитемией, резистентной к другим видам лечения.
Удаление тромбоцитов (тромбоцитоферез) применяли в редких случаях у больных с серьезными внутренними кровоизлияниями, при рецидивирующих тромбозах или перед неотложной хирургической операцией, для того чтобы быстро уменьшить количество тромбоцитов. Однако тромбоцитоферез редко необходим. Эти эффекты транзиторные с быстрым восстановлением количества тромбоцитов. Гидроксимочевина или анагрелид не дают немедленный эффект, но начать использовать их необходимо одновременно с тромбоцитоферезом.
Ключевые моменты относительно эссенциального тромбоцитоза
Эссенциальная тромбоцитемия представляет собой клональную аномалию мультипотентных гемопоэтических стволовых клеток, которая приводит к увеличению количества тромбоцитов.
Пациенты находятся под угрозой тромбоза микрососудов, кровоизлияний, и редко макрососудистого тромбоза.
Эссенциальная тромбоцитемия диагностируется методом исключения, в частности, должны быть исключены другие миелопролиферативные неоплазии и реактивный (вторичный) тромбоцитоз.
Для пациентов с асимптоматическим течением болезни терапия не требуется. Аспирин, как правило, эффективен при микрососудистых нарушениях (глазной мигрени, эритромегалии и транзиторных ишемических атаках).
Чтобы контролировать количество тромбоцитов для некоторых пациентов с тяжелым тромбоцитозом может потребоваться более агрессивное лечение; такие меры включают использование гидроксимочевины, анагрелида, интерферона альфа-2b и тромбоцитофереза.
Тромбоцитоз
Тромбоцитоз – это патологическое состояние, характеризующееся увеличением содержания в крови тромбоцитов. Причиной данного явления выступают инфекционные, воспалительные или аутоиммунные патологии, а также злокачественные опухоли кроветворной системы. У детей часто возникает на фоне железодефицитной анемии. Клиническая картина может быть различной и определяется основным заболеванием. Уровень кровяных пластинок, как часть общего анализа крови, исследуется в венозной или капиллярной крови. Для коррекции тромбоцитоза проводится лечение болезни, на фоне которой он развился.
Классификация
Верхняя граница нормального значения тромбоцитов варьирует от 350 000 до 400 000 в 1 мкл в зависимости от референсных интервалов конкретной лаборатории, выполняющей анализ. По степени увеличения различают следующие виды тромбоцитоза:
Причиной экстремального и тяжелого тромбоцитоза выступают онкогематологические патологии. По происхождению тромбоцитозы бывают:
Причины тромбоцитоза
Физиологические состояния
Повышенный уровень тромбоцитов не всегда свидетельствует о патологии. Существует физиологический (кратковременный, транзиторный) тромбоцитоз, обусловленный различными обстоятельствами, например, стрессом, интенсивной физической нагрузкой. Причиной является мобилизация кровяных пластинок, а точнее их переход от краевого стояния к центральному кровотоку в сосудах селезенки, легких.
Кроме того, незначительный физиологический тромбоцитоз наблюдается у детей, начиная с периода новорожденности до 11 лет. Также существует так называемый гемоконцентрационный тромбоцитоз, причиной которого является обезвоживание. Данное явление обусловлено уменьшением объема жидкой части крови (плазмы) и относительным повышением форменных элементов (тромбоцитов, эритроцитов, лейкоцитов). В этой ситуации необходимо ориентироваться на гематокрит – при обезвоживании он повышен.
Инфекции
Это наиболее частая причина тромбоцитоза (около 40%). Повышение уровня кровяных пластинок развивается при:
Существует два патогенетических механизма развития тромбоцитоза в ответ на инфекционное заболевание. Во-первых, во время борьбы с патогенами, лейкоциты продуцируют большое количество медиаторов воспаления, в том числе интерлейкина-6, который стимулирует костномозговой мегакарицитопоэз (образование предшественников тромбоцитов). Во-вторых, тромбоциты сами являются частью противоинфекционного иммунитета – они способны вырабатывать бактерицидные вещества, захватывать, нейтрализовывать, даже фагоцитировать некоторые виды бактерий, вирусов, чужеродных частиц.
Тромбоциты облегчают миграцию лейкоцитов к очагу инфекционного воспаления путем взаимодействия с эндотелиальными клетками сосудистой стенки. Тромбоцитоз при инфекциях возникает резко, коррелирует с тяжестью болезни, быстро разрешается после элиминации патогена из организма и стихания воспалительного процесса. Тромбоцитоз обычно мягкий или умеренный, при септическом состоянии может доходить до тяжелой степени, у детей несколько выраженнее, чем у взрослых.
Аутоиммунные заболевания
Другой частой причиной тромбоцитоза считаются хронические ревматологические патологии, протекающие с аутоиммунным воспалением. Механизм увеличения содержания кровяных пластинок заключается в гиперпродукции таких веществ, как интерлейкин-6, колониестимулирующие факторы, которые активизируют костномозговое тромбоцитообразование. Степень тромбоцитоза соответствует активности воспаления (минимальный в стадию ремиссии, максимальный во время рецидива).
При таких болезнях как ревматоидный артрит, системная красная волчанка (СКВ), воспалительные заболевания кишечника (болезнь Крона, неспецифический язвенный колит) наблюдается мягкая либо умеренная степень. При системных васкулитах с некротизирующей деструкцией стенок сосудов встречается тяжелый тромбоцитоз, так как при васкулитах, помимо прочих воспалительных медиаторов, в большом количестве синтезируется фактор некроза опухолей, также оказывающий стимулирующий эффект на тромбоцитообразование. Особенно часто высокие цифры тромбоцитов наблюдаются у детей.
Анемии
Нередко причиной тромбоцитоза, особенно у детей, выступает железодефицитная анемия. Точные механизмы этого явления до сих пор не выяснены, однако точно установлена обратная взаимосвязь между сниженными показателями метаболизма железа (ферритина, железосвязывающей способности сыворотки) и завышенным уровнем кровяных пластинок. Предполагается, что железо обладает подавляющим эффектом на созревание мегакариоцитов (клеток-предшественников).
Кроме того, часть плюрипотентных стволовых клеток костного мозга в условиях дефицита железа не способна превращаться в эритроциты. В результате происходит своеобразное «шунтирование» и больший процент стволовых клеток начинает созревать по мегакариоцитарному пути. Тромбоцитоз при железодефицитной анемии мягкий, иногда умеренный. Тромбоциты быстро приходят в норму после коррекции дефицита железа, увеличения гемоглобина.
Однако при усугублении анемии уровень тромбоцитов падает до состояния тромбоцитопении. Причиной железодефицита могут быть недостаток железа в пище, повышенный расход железа (период роста у детей, беременность, лактация) либо хронические кровопотери (длительные менструации, кровотечения из желудочно-кишечного тракта при язвенной болезни желудка).
Злокачественные болезни крови
Причиной примерно 15% всех тромбоцитозов являются гемобластозы – хронический миелоидный лейкоз, Ph-негативные миелопролиферативные патологии (эссенциальная тромбоцитемия, истинная полицитемия, а также первичный миелофиброз). Увеличение числа кровяных пластинок при этих болезнях обусловлено клональной (опухолевой) трансформацией мегакариоцитарного ростка костного мозга вследствие различных мутаций, что приводит к гиперпродукции тромбоцитов.
Данные болезни чаще встречаются у взрослых и людей пожилого возраста, у детей – лишь в исключительных случаях. Вначале тромбоцитоз умеренный, по мере прогрессирования он нарастает, достигая тяжелой или экстремальной степени, из-за чего часто возникают нарушения микроциркуляции, артериальные, венозные тромбозы различной локализации. Концентрация кровяных пластинок нормализуется очень медленно, только после курсов специфического миелосупрессивного лечения.
Спленэктомия
Селезенка, являясь органом, депонирующим кровь, удерживает большое количество форменных элементов, включая тромбоциты. Также селезенка принимает непосредственное участие в тромбоцитопоэзе, секретируя гормоны тромбоцитопенин, спленин, подавляющие костномозговое созревание мегакариоцитов. Поэтому тромбоцитоз после спленэктомии обусловлен двумя механизмами: выходом в циркулирующую кровь тромбоцитов, в норме находящихся в селезеночном депо, и феноменом «растормаживания костного мозга», т.е. усилением продукции тромбоцитов.
Увеличение количества кровяных пластинок возникает не сразу, а примерно через неделю после спленэктомии, достигает максимума к 13-14 дню (до 700-800 тыс.), нередко становясь причиной венозного тромбоза воротной вены, а затем медленно возвращается к норме за несколько недель или месяцев.
Травмы и операции
Массивное повреждение тканей (рана при полостной операции, перелом, обширные ожоги) вызывает активацию свертывающей системы крови, а именно сосудисто-тромбоцитарного звена, являющегося первым этапом гемостаза. Он подразумевает спазм сосудов, а также адгезию и агрегацию тромбоцитов в месте повреждения сосудистой стенки. Расход тромбоцитов стимулирует их активный выход из депо и компенсаторное усиление их костномозговой продукции. Объем повреждения коррелирует со степенью тромбоцитоза. Данный вид тромбоцитоза обычно не требует лечения.
Онкологические заболевания
Причиной тромбоцитоза при солидных (негемопоэтических) опухолях является способность раковых клеток продуцировать интерлейкин-6, стимулирующий тромбоцитопоэз. Такая особенность обнаружена при мелкоклеточном раке легких, аденокарциноме ободочной кишки, злокачественной мезотелиоме. Кроме того, распад опухоли часто вызывает кровотечения, приводя к железодефицитной анемии. Степень тромбоцитоза обычно умеренная, у детей может быть тяжелой, регрессирует после долгого лечения химиотерапевтическими средствами.
Редкие причины
Диагностика
Тромбоцитоз выявляется в клиническом анализе крови. Хотя очень высокие показатели тромбоцитов чаще наблюдаются при гематологических заболеваниях, лишь по одному только уровню кровяных пластинок невозможно определить причину тромбоцитоза. Поэтому при его обнаружении следует посетить терапевта. Врач внимательно расспрашивает о жалобах пациента, давности возникновения симптомов, проводит общий осмотр больного. Затем на основании полученных данных назначается дополнительное обследование, включающее:
Коррекция
Консервативная терапия
В большинстве случаев, чтобы скорректировать тромбоцитоз, достаточно искоренения причины, т.е. лечения основного заболевания. Кратковременный тромбоцитоз, развившийся на фоне стресса или введения лекарственных препаратов, не требует вмешательства. При стойком длительном тромбоцитозе необходима консультация гематолога для выявления причины, назначения соответствующего лечения. Терапия тромбоцитозов имеет несколько направлений, включающих:
Специализированное лечение
Единственный метод, позволяющий добиться полного исцеления от злокачественного гематологического заболевания – это аллогенная трансплантация костного мозга. Для этого необходимо проведение HLA-типирования для подбора совместимого донора. Однако по причине высокого риска развития жизнеугрожающих осложнений к данному способу прибегают только при неэффективности консервативного лечения.
Прогноз
Исход зависит как от основной патологии, так и от степени тромбоцитоза. Например, острая вирусная инфекция, железодефицитная анемия характеризуются доброкачественным течением. Больные эссенциальной тромбоцитемией при грамотном подборе патогенетического и симптоматического лечения могут прожить больше 80 лет. Люди с хроническим миелолейкозом, напротив, живут около 5-10 лет с момента постановки диагноза.
Так как у детей почти всегда встречается реактивный тромбоцитоз, у них прогноз благоприятный. Для мягкого и умеренного тромбоцитоза нетипично тромбообразование. При экстремальной или тяжелой степени существует очень большая вероятность фатальных тромбозов, приводящих к инфаркту миокарда, легкого, ишемическому инсульту.
Эссенциальный тромбоцитоз что это такое и как лечить
Эссенциальная тромбоцитемия (ЭТ) является клоновым хроническим миелопролиферативным заболеванием (ХМПЗ) с преимущественной пролиферацией мегакариоцитов и повышенным образованием тромбоцитов (более 400*109/л). Синонимы — первичная тромбоцитемия, идиопатическая тромбоцитемия, геморрагическая тромбоцитемия. В классификации хронических гемобластозов, предложенной А. И. Воробьевым и М. Д. Бриллиант, данное заболевание обозначается как хронический мегакарио-цитарный лейкоз.
Эссенциальная тромбоцитемия — сравнительно доброкачественное заболевание с нормальной продолжительностью жизни больных, если она не прерывается фатальными сосудистыми осложнениями.
Истинная частота эссенциальной тромбоцитемии неизвестна, поскольку соответствующие эпидемиологические исследования не проводились. Принято считать, что это одно из самых редких ХМПЗ. Оно встречается в 4 раза реже, чем истинная полицитемия. В классификации ВОЗ (2001) указывается, что ежегодная заболеваемость эссенциальной тромбоцитемии составляет 1—2,5 на 100 000 населения.
Пик заболеваемости приходится на возраст 50—60 лет, но не является редкостью заболевание в молодом и даже детском возрасте. Связь частоты болезни с полом неясна. Некоторые авторы указывают на более частую заболеваемость лиц женского пола по сравнению с мужчинами (2,9:1)]. Известны случаи семейной эссенциальной тромбоцитемии в нескольких поколениях.
К настоящему времени установлено, что семейная тромбоцитемия — это самостоятельное, неклональное заболевание, связанное с мутациями гена рецептора тромбопоэтина — Mpl, приводящими к повышенной чувствительности метакариоцитов к тромбопоэтину (ТРО) [70]. Установлены 4 различные мутации гена рецептора тромбопоэтина при семейной тромбоцитемии, в 3 из них механизм возникновения тромбоцитоза исследован на молекулярном уровне.
Обнаружено увеличение трансляционной способности мРНК в связи с мутацией в домене гена ТРО, осуществляющем в норме физиологическое ингибирование трансляции. Заболевание наследуется по аутосомно-доминантному типу, тромбоцитоз обнаруживается уже у новорожденных. Клиническое течение заболевания мягкое. Сосудистые осложнения возможны, но не часты, лейкемической трансформации не наблюдается. Следует отметить, что тромбоцитоз у детей может быть и проявлением врожденного ХМПЗ.
Патогенез эссенциальной тромбоцитемии (ЭТ)
Клональная неопластическая природа заболевания была доказана вначале при исследовании типов Г-6-ФДГ у гетерозиготных по этому ферменту женщин-мулаток, больных эссенциальной тромбоцитемией (ЭТ), а позднее подтверждена при изучении инактивации Х-хромосомы.
С самого начала исследований было обнаружено, что гемопоэз при эссенциальной тромбоцитемии моноклонален лишь у части больных. Так, в исследовании P. Chiusolo и соавт. моноклональный гемопоэз был обнаружен у 39,2 % из 56 исследованных больных, у остальных он был поликлональным.
Не установлено перехода поликлонального гемопоэза в моноклональный при длительном наблюдении. На этом основании высказывается предположение, что эссенциальная тромбоцитемия — гетерогенное заболевание с различными молекулярными механизмами у больных с моно- и поликлональным гемопоэзом, приводящими к избирательному увеличению числа тромбоцитов в обеих подгруппах. Эту концепцию подтверждают и результаты исследования гена PRV-1, экспрессия которого повышена лишь у больных при постоянном тромбоцитозе с моноклональным гемопоэзом, и спонтанного образования эритроидных колоний, также отмечаемого лишь у больных с моноклональным гемопоэзом.
Выявлены различия и в частоте сосудистых осложнений: значительной у больных с моноклональным гемопоэзом и небольшой — с поликлональным. Тромбозы в системе чревных сосудов, портальной и надпеченочной вен встречаются, например, только в группе больных с моноклональным гемопоэзом. Молекулярные механизмы, лежащие в основе тромбоцитоза в обеих подгруппах эссенциальной тромбоцитемии, пока не известны.
Когда констатируется моноклональность, она касается клеток-предшественников всего гемопоэза (С34+), а не предшественников лишь мегакариоцитарного ростка.
При эссенциальной тромбоцитемии (ЭТ) в крови обнаружено статистически достоверное увеличение содержания тромбопоэтина и фактора роста гепатоцитов (HGF). Этот фактор, по всей вероятности, играет существенную роль в пролиферативной активности мегакариоцитов. В то время как корреляции между числом тромбоцитов, лейкоцитов и уровнем ТРО в сыворотке больных ЭТ не установлено, найдена достоверная корреляция между указанными показателями и уровнем HGF.
При эссенциальной тромбоцитемии (ЭТ) в культуральной среде, содержащей сыворотку крови, мегакариоциты растут без добавления ТРО, в средах без сыворотки демонстрируют гиперчувствительность к тромбопоэтину, а также близкому к нему фактору роста и развития тромбоцитов (MGDF). Показано, что тромбоциты при эссенциальной тромбоцитемии (ЭТ) в 50 раз более чувствительны к MGDF, чем тромбоциты здоровых людей.
При эссенциальной тромбоцитемии (ЭТ) нередко наблюдается также спонтанное образование эритроидных колоний, свойственное истинной полицитемии, что, вероятно, является отражением общности дефекта клеток-предшественников при обоих заболеваниях. Патогенетическая близость эссенциальной тромбоцитемии, истинной полицитемии и хронического идиопатического миелофиброза следует и из факта частого обнаружения экспрессии гена PRV-1 при всех 3 заболеваниях, в 77, 86 и 100 % соответственно. Имеются различия в уровне экспрессии этого гена: при истинной полицитемии (ИП) он самый высокий.
Сравнительное изучение роста мегакариоцитарных и эритроидных предшественников в культуре, экспрессии гена PRV-1 и клональности гемопоэза при эссенциальной тромбоцитемии и истинной полицитемии показали, что при ИП эндогенный рост эритроидных колоний наблюдается в 100 % случаев, мегакариоцитарных колоний — у 4 из 11 больных; моноклональность обнаруживается в 50 %, а повышенная экспрессия гена PRV-1 — y 91 % больных. При эссенциальной тромбоцитемии эти показатели составляют соответственно 29, 53, 43 и 59 %.
Обнаружено снижение уровня экспрессии Mpl более чем у 90 % больных эссенциальной тромбоцитемией по сравнению со здоровыми и больными с реактивным тромбоцитозом, однако корреляции между уровнем экспрессии рецептора и количеством тромбоцитов, а также клиническим течением эссенциальной тромбоцитемии не было обнаружено. В то же время роль рецептора Mpl в развитии гипертромбоцитоза подтверждена следующим фактом: обнаружено, что при замене одного нуклеотида в результате точечной мутации у некоторых больных рецептор Mpl изменен и представляет собой K39N-Mpl.
Гетерозиготность, когда один из генов Mpl является нормальным, а второй — K39N-Mpl, сопровождается статистически достоверным более высоким уровнем тромбоцитоза по сравнению с количеством тромбоцитов у 100 пациентов с другим типом гена Mpl. У двух больных была обнаружена гомозиготность, оба аллеля гена тромбопоэтинового рецептора являлись K39N-Mpl, у обоих больных был постоянный высокий тромбоцитоз со средним количеством тромбоцитов 850*109/л.
Исследование уровня ИЛ-6, который участвует в созревании мегакариоцитов, показало, что он всегда снижен у больных эссенциальной тромбоцитемией и значительно повышен у 80 % больных с реактивными тромбоцитозами.
Недавно было установлено, что уровень экспрессии определенных генов, кодирующих тромбоцитарные гликопротеины, у здоровых лиц и у больных эссенциальной тромбоцитемией различен и может служить тестом для разграничения моно- и поликлонального гемопоэза при заболеваниях с увеличенным количеством тромбоцитов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021